第二部【企業情報】
第1【企業の概況】
1【主要な経営指標等の推移】
提出会社の状況
|
回次 |
第3期 |
第4期 |
第5期 |
第6期 |
第7期 |
|
|
決算年月 |
2016年12月 |
2017年12月 |
2018年12月 |
2019年12月 |
2020年12月 |
|
|
売上高 |
(千円) |
|
|
|
|
|
|
経常利益又は 経常損失(△) |
(千円) |
△ |
△ |
△ |
△ |
|
|
当期純利益又は 当期純損失(△) |
(千円) |
△ |
△ |
△ |
△ |
|
|
持分法を適用した場合の投資利益 |
(千円) |
|
|
|
|
|
|
資本金 |
(千円) |
|
|
|
|
|
|
発行済株式総数 |
(株) |
|
|
|
|
|
|
普通株式 |
|
|
|
|
|
|
|
A種種類株式 |
|
|
|
|
|
|
|
B種種類株式 |
|
|
|
|
|
|
|
C種種類株式 |
|
|
|
|
|
|
|
純資産額 |
(千円) |
|
|
|
|
|
|
総資産額 |
(千円) |
|
|
|
|
|
|
1株当たり純資産額 |
(円) |
△ |
△ |
△ |
|
|
|
1株当たり配当額 |
(円) |
|
|
|
|
|
|
(うち1株当たり中間配当額) |
( |
( |
( |
( |
( |
|
|
1株当たり当期純利益又は1株当たり当期純損失(△) |
(円) |
△ |
△ |
△ |
△ |
|
|
潜在株式調整後1株当たり当期純利益 |
(円) |
|
|
|
|
|
|
自己資本比率 |
(%) |
|
|
|
|
|
|
自己資本利益率 |
(%) |
|
|
|
|
|
|
株価収益率 |
(倍) |
|
|
|
|
|
|
配当性向 |
(%) |
|
|
|
|
|
|
営業活動による キャッシュ・フロー |
(千円) |
|
|
|
△ |
△ |
|
投資活動による キャッシュ・フロー |
(千円) |
|
|
|
△ |
△ |
|
財務活動による キャッシュ・フロー |
(千円) |
|
|
|
|
|
|
現金及び現金同等物の期末残高 |
(千円) |
|
|
|
|
|
|
従業員数 |
(人) |
|
|
|
|
|
|
(外、平均臨時雇用者数) |
( |
( |
( |
( |
( |
|
(注)1.当社は連結財務諸表を作成しておりませんので、連結会計年度に係る主要な経営指標等の推移については記載しておりません。
2.売上高には、消費税等は含まれておりません。
3.持分法を適用した場合の投資利益については、関連会社が存在しないため記載しておりません。
4.1株当たり純資産額の計算にあたっては、次の方法により算定しております。
第3期につき、事業年度末の純資産の部の合計額よりA種種類株式及びB種種類株式の払込金額を控除し、1株当たり純資産額を算定しております。第4期、第5期、第6期及び第7期につき、事業年度末の純資産の部の合計額よりA種種類株式、B種種類株式及びC種種類株式の払込金額を控除し、1株当たり純資産額を算定しております。
5.潜在株式調整後1株当たり当期純利益については、第3期、第4期、第5期及び第6期につき、潜在株式は存在するものの、当社株式は非上場であり、期中平均株価が把握できないため、また、1株当たり当期純損失であるため、記載しておりません。第7期につき潜在株式は存在するものの、当社株式は非上場であり、期中平均株価が把握できないため、記載しておりません。
6.第3期、第4期、第5期及び第6期の自己資本利益率については、当期純損失を計上しているため、記載しておりません。
7.株価収益率については、当社株式は非上場であるため、記載しておりません。
8.当社は配当を行っておりませんので、1株当たり配当額及び配当性向については、それぞれ記載しておりません。
9.第3期、第4期及び第5期についてはキャッシュ・フロー計算書を作成しておりませんので、キャッシュ・フローに係る各項目については記載しておりません。
10.第6期及び第7期の財務諸表については、「財務諸表等の用語、様式及び作成方法に関する規則」(昭和38年大蔵省令第59号)に基づき作成しており、金融商品取引法第193条の2第1項の規定に基づき、EY新日本有限責任監査法人の監査を受けております。
なお、第3期、第4期及び第5期については、「会社計算規則」(平成18年法務省令第13号)の規定に基づき算出した各数値を記載しております。また、当該各数値については、金融商品取引法第193条の2第1項の規定に基づくEY新日本有限責任監査法人の監査を受けておりません。
11.当社は、株主の株式取得請求権の行使を受けたことにより、2021年11月29日付でA種種類株式、B種種類株式及びC種種類株式の全てを自己株式として取得し、対価として普通株式を交付しております。また、当社が取得したA種種類株式、B種種類株式及びC種種類株式の全てについて、2021年11月12日開催の取締役会決議により2021年11月29日付で消却しております。なお、当社は、2021年11月30日開催の臨時株主総会決議により、種類株式を発行する旨の定款の定めを廃止しております。
12.当社は、2021年11月12日開催の取締役会決議により、2021年11月30日付で普通株式1株につき1,500株の割合で株式分割を行っております。第6期の期首に当該株式分割が行われたと仮定し、1株当たり純資産額及び1株当たり当期純利益又は1株当たり当期純損失を算定しております。
13.当社は、2021年11月30日付で普通株式1株につき1,500株の割合で株式分割を行っております。
そこで、東京証券取引所自主規制法人(現 日本取引所自主規制法人)の引受担当者宛通知「『新規上場申請のための有価証券報告書(Ⅰの部)』の作成上の留意点について」(2012年8月21日付東証上審第133号)に基づき、第3期の期首に当該株式分割が行われたと仮定して算出した場合の1株当たり指標の推移を参考までに掲げると、以下のとおりとなります。
なお、第3期、第4期及び第5期の数値(1株当たり配当額についてはすべての数値)については、EY新日本有限責任監査法人の監査を受けておりません。
|
回次 |
第3期 |
第4期 |
第5期 |
第6期 |
第7期 |
|
決算年月 |
2016年12月 |
2017年12月 |
2018年12月 |
2019年12月 |
2020年12月 |
|
1株当たり純資産額 (円) |
△85.38 |
△151.84 |
△225.41 |
17.66 |
54.41 |
|
1株当たり当期純利益又は 1株当たり当期純損失(△) (円) |
△104.06 |
△164.00 |
△167.37 |
△99.74 |
10.88 |
|
潜在株式調整後1株当たり 当期純利益 (円) |
- |
- |
- |
- |
- |
|
1株当たり配当額 (うち1株当たり中間配当額) (円) |
- (-) |
- (-) |
- (-) |
- (-) |
- (-) |
2【沿革】
(1)当社創業の経緯
当社の代表取締役会長である鈴木隆二は、研究者としてのキャリアを開始して以来30年以上一貫して、免疫システムの本質を明らかにするというテーマに取り組んでまいりました。免疫システムには、免疫細胞が細菌やウイルスなどの病原体や、がん細胞などの異常な細胞を認識して攻撃することによって、生体を病気から保護するという有益な点がある反面、自己の細胞であるにも関わらず異物として間違って攻撃をしてしまう自己免疫疾患や、生体にとって無害な物質に対しても過剰に応答してしまうアレルギーを引き起こすなどの負の側面もあります。
鈴木はこの複雑な免疫システムを詳細に解析することができれば、感染症やがん、自己免疫疾患、アレルギーなどの免疫システムが関与するほとんど全ての疾患に対する、これまでにない新しい薬や新しい治療法・診断法の開発など、多くの面で医療の発展に寄与することができると信じて開発を続けた結果、当社独自の免疫多様性解析技術を完成させることができました。
そして、鈴木は熟考の上、この免疫多様性解析技術を企業として事業化することが、世界中の病気で苦しむ患者さんに対する新しい薬や新しい治療法・診断法を実現させる最短の道となると考えて、2014年10月に当社を大阪府茨木市で創業いたしました。
(2)当社の沿革
当社設立以降の沿革は、以下のとおりであります。
|
年月 |
概要 |
|
2014年10月 |
大阪府茨木市にRepertoire Genesis株式会社を設立 |
|
2014年11月 |
大阪府茨木市に所在する彩都バイオインキュベータに研究所を開設 |
|
2014年12月 |
免疫多様性解析サービスを開始 |
|
2015年6月 |
和光純薬工業株式会社(現 富士フイルム和光純薬株式会社)と受託サービス仲介契約を締結し、同社を日本国内における販売代理店に指定 |
|
2016年5月 |
東京都千代田区に東京オフィスを開設 |
|
2017年3月 |
がん免疫療法に対する新規バイオマーカー(注1)に関する新規特許を学校法人兵庫医科大学と共同で出願 |
|
2017年4月 |
解析依頼数の増加と研究開発の拡大に対応するために研究所を増床 |
|
2017年6月 |
免疫多様性解析に関する基本特許が日本国内で成立(特許第6164759号) |
|
2017年10月 |
新規細胞治療に寄与するT細胞受容体(注2)の完全置換に関する特許2件を国立大学法人広島大学と共同で出願 |
|
2018年8月 |
筋痛性脳脊髄炎/慢性疲労症候群(ME/CFS)に対するバイオマーカーに関する新規特許を国立研究開発法人国立精神・神経医療研究センターと共同で出願 |
|
シングルセル(注3)からのTCR/BCRペア遺伝子(注4)の増幅技術に関する新規特許を単独で出願 |
|
|
2018年10月 |
解析機能及び研究機能のさらなる強化のため研究所を増床 |
|
2018年11月 |
東京都中央区に東京オフィスを移転 |
|
2019年3月 |
当社研究所がTCR/BCRレパトア解析(注5)を対象として国際規格「ISO/IEC17025:2017」(注6)の認定を取得 |
|
2019年9月 |
全薬工業株式会社と包括的な共同研究開発契約の締結及び資本提携を実施 |
|
英 QIAGEN社とコンパニオン診断薬(注7)の開発及び商業化において、全世界を対象とした非独占契約を締結 |
|
|
2019年10月 |
国立大学法人広島大学の原爆放射線医科学研究所内に「次世代ゲノム細胞創薬共同研究講座」を開設 |
|
2020年3月 |
仏 Cellectis社とのTALヌクレアーゼ技術(注8)を用いたコラボレーション及びライセンスオプション契約を締結 |
|
2020年5月 |
ネオエピトープ解析(注9)に関する基本特許が日本国内で成立(特許第6710004号) |
|
2020年6月 |
国立研究開発法人日本医療研究開発機構(以下「AMED」という。)のプロジェクトである「ハイリスク患者選別のためのCOVID-19ウイルス抗原特異的免疫応答の網羅的評価法」の開発へ参画 |
|
産学官連携による高機能ゲノム編集T細胞の製造基盤技術の確立に向けてAMEDと委託研究開発契約を締結 |
<用語解説>
|
(注1) |
バイオマーカー |
体液や組織に含まれる物質で、病気の変化や治療に対する反応に相関し指標となるもののこと。疾患の診断のための診断マーカー、経過を予測する予後マーカー、薬剤がどう作用するかを診る薬力学マーカー、ある治療による効果を予測する予測マーカー等に目的別に分類される。 |
|
(注2) |
T細胞受容体(TCR) |
T細胞表面に存在する受容体分子。T細胞受容体(TCR、T-Cell Receptor)は、細胞膜表面に存在するMHCというタンパク質上に提示されたペプチドを認識することで活性化される。 |
|
(注3) |
シングルセル |
シングルセル(単一細胞)という意味。シングルセル単位でDNAの状態やメッセンジャーRNAの発現量などを解析する手法をシングルセル解析という。 |
|
(注4) |
TCR/BCRペア遺伝子 |
T細胞表面に存在する受容体分子(TCR、T-Cell Receptor)とB細胞表面に存在する受容体(BCR、T-Cell Receptor)はそれぞれ2種類のタンパク質の部品から構成されるがそのタンパク質の組み合わせ(ペア)の元となる遺伝子を解析する手法のこと。 |
|
(注5) |
TCR/BCRレパトア解析 |
様々な生体情報の多様性を解析すること(レパトアは元々英語のレパートリーと同義のフランス語)。TCR/BCRレパトア解析とはTCRとBCRの多様性を解析すること。 |
|
(注6) |
国際規格「ISO/IEC17025:2017」 |
「ISO/IEC 17025:2017」は、スイスのジュネーブに在る国際標準化機構が策定している国家間に共通な標準規格のうちの一つ。特定の種類の試験及び校正を実施する試験所の技術能力を証明するもので、ISO9001で要求される品質マネジメントに関する要件に加えて、試験を正しく実施する技術力があることが要求されている。 |
|
(注7) |
コンパニオン診断薬 |
ある治療が効果があるかどうかを治療の前にあらかじめ検査することをコンパニオン診断といい、その診断のために使う薬をコンパニオン診断薬という。 |
|
(注8) |
TALヌクレアーゼ技術 |
ゲノム上の任意の配列を切断できるヌクレアーゼ(TALEN)を用いたゲノム編集技術のこと。 |
|
(注9) |
ネオエピトープ解析 |
がん細胞などの病気の細胞のみに存在している、正常な細胞とは異なる変異ペプチド(ネオエピトープ)を正確に判定する技術。 |
3【事業の内容】
当社は、「治らないをなくす」というミッションのもと、当社独自の免疫多様性解析技術から得られる多くの情報を統合し、生体反応を多方面から正確に把握することで、がんや自己免疫疾患、感染症などの幅広い疾患分野において、免疫系を応用したこれまでにない新しい医療開発(基礎研究、予防、診断、治療)を支援する事業を展開しております。
<当社事業の概念図>
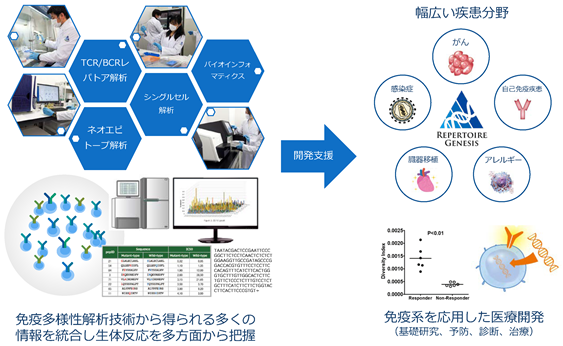
免疫系は、私たちが体内に元々備えている自然界で最も洗練された診断及び治療の仕組みの一つと言えます。しかしながら、これまではその詳細を十分に把握/解明できなかったため、医療分野では免疫系が持つ潜在的な医療応用へのポテンシャルを十分に活かせていませんでした。
当社独自の免疫多様性解析技術は、患者さんの免疫系に関する複雑かつ多くの情報を遺伝子レベルで解読し、免疫系がその患者さんの病気にどのように関与しているか、また特定の治療方法がどのように免疫系に影響を与えているかの検証を可能とします。これらの解析結果を独自のバイオインフォマティクス(注1)技術とこれまでに当社が蓄積したデータベースと組み合わせて多面的に把握することで、顧客の抱える医療開発に関する課題に合わせた高付加価値なソリューションが提供可能となります。
当社では2014年10月の創業以来、免疫系を担う主要なリンパ球(注2)であるT細胞(注3)の表面にあるT細胞受容体(TCR)(注4)及びB細胞(注5)の表面にあるB細胞受容体(BCR)(注6)の詳細な遺伝子解析であるTCR/BCRレパトア解析(注7)を主軸として、がん、感染症、自己免疫疾患などの多くの疾患分野での解析を実施してきております。これまでに多くのアカデミア(大学や研究機関)や製薬企業との共同研究やパートナーシップ、及び商業的関係構築の実績を積み上げてきました。当社は今後も多くの研究機関と協力することで、免疫系への理解を深めて、「治らないをなくす」という世界を実現すべく、当社独自の免疫多様性解析技術を世の中に広めていくことで、人類の健康に資する研究開発を推進することを目的とした事業展開をしていきます。
<用語解説>
|
(注1) |
バイオインフォマティクス |
生命科学と情報科学の融合分野の一つ。DNAやRNA、タンパク質をはじめとする生命が持つ様々な「情報」を対象にして、情報科学や統計学などのアルゴリズムを用いた分析から生命現象を解き明かしていくことを目的とする。 |
|
(注2) |
リンパ球 |
白血球の成分の一種であり、生体が引き起こす免疫反応に関与する細胞。機能面から、T細胞、B細胞、NK細胞などに分類される。 |
|
(注3) |
T細胞 |
リンパ球の一種で、生体内で細胞性免疫を担う細胞。細胞表面にT細胞受容体(TCR)を有し、特定の抗原(注13を参照)を特異的に認識する。免疫系を調節するヘルパーT細胞と、ウイルス等に感染した自己細胞を攻撃する細胞傷害性T細胞に大別される。 |
|
(注4) |
T細胞受容体(TCR) |
T細胞表面に存在する受容体分子。T細胞受容体(TCR、T-Cell Receptor)は、細胞膜表面に存在するMHCというタンパク質上に提示されたペプチドを認識することで活性化される。 |
|
(注5) |
B細胞 |
リンパ球の一種で、生体内で抗体産生を担う細胞。抗原と特異的に結合する抗体を作ることで、異物を排除するように働く。 |
|
(注6) |
B細胞受容体(BCR) |
B細胞表面に存在する受容体分子。B細胞受容体(BCR、B-Cell Receptor)は、抗原を認識することで活性化されるとともに細胞外へ分泌されて抗体として働く。 |
|
(注7) |
レパトア解析 |
様々な生体情報の多様性を解析すること(レパトアは元々英語のレパートリーと同義のフランス語)。TCR/BCRレパトア解析とはTCRとBCRの多様性を解析すること。 |
(1) 当社の事業領域
① 拡大を続ける事業機会
当社がターゲットとする免疫系を応用した医療開発領域は、英国ロンドンに本社を置き、ライフサイエンス分野におけるマーケット情報分析を行うEvaluate社によると、下記のグラフのとおり、がん治療薬、糖尿病治療薬、免疫抑制剤及びワクチンにおいて全世界の売上の増加が予測されるなど、ヘルスケア分野において大きな拡大が想定される成長マーケットの一つであり、当社は免疫応答を詳細に把握することができる当社独自の免疫多様性解析技術を活用することで、がん、感染症、自己免疫疾患、アレルギー、臓器移植など数多くの免疫系が関与する疾患分野にアプローチすることを目指しております。
<免疫系を応用した主要な治療分野ごとの世界の治療薬売上予測>
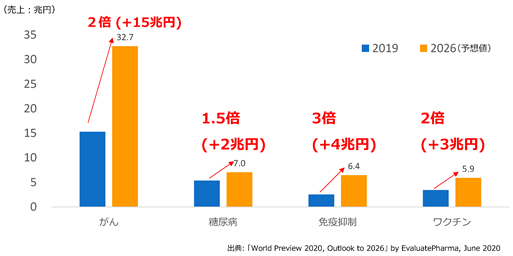
また、新型コロナウイルス感染症(COVID-19)等の感染症の大流行への対策が、持続可能な社会を実現するための大きな社会課題となる中、感染症予防ワクチンの開発支援や感染による重症化を予測するバイオマーカー(注8)の開発※1など当社が寄与できる事業機会が拡大してきております。また、がん免疫療法、自己免疫疾患市場の拡大、抗体医薬、免疫細胞療法、遺伝子治療の普及、ゲノム編集(注9)の臨床応用の試みが加速化する中で、当社が保有する一連の独自技術を組み合わせることで、製薬企業による新規抗体医薬の創出、既存薬剤の適応拡大の支援、ゲノム編集を用いた免疫細胞療法(TCR-T(注10)、CAR-T(注11))の開発も可能となります。さらに、近年では製薬企業による診断薬や予防分野への参入、後発医薬品メーカーの新薬開発への参入、AI創薬(注12)の試みの活発化など、創薬環境が大きく変化してきている中で、当社では免疫細胞の受容体情報から潜在的なバイオマーカーを見出し、診断アプリケーションの開発に迅速につなげ、また免疫系が持つ、病気の監視、早期発見、治療機能を応用した創薬支援サービスを提供し、複雑な免疫系の暗号を復号化し、病気の診断と治療を変革するためのバイオインフォマティクスを軸とした創薬ソリューションを提供するなど、外部環境の変化を捉えた事業展開を行っております。
※1:国立研究開発法人日本医療開発研究機構(AMED)採択課題:ハイリスク患者選別のためのCOVID-19ウイルス抗原特異的免疫応答の網羅的評価法の開発

<用語解説>
|
(注8) |
バイオマーカー |
体液や組織に含まれる物質で、病気の変化や治療に対する反応に相関し指標となるもののこと。疾患の診断のための診断マーカー、経過を予測する予後マーカー、薬剤がどう作用するかを診る薬力学マーカー、ある治療による効果を予測する予測マーカー等に目的別に分類される。 |
|
(注9) |
ゲノム編集 |
DNA切断酵素を利用して、ゲノム上の標的遺伝子を改変する技術のこと。ゲノムとは、DNAに含まれる遺伝情報全体のこと。 |
|
(注10) |
TCR-T |
がん免疫療法の一種であり、T細胞が持つTCR(T細胞受容体)遺伝子を改変することで、改変されたT細胞が、がん細胞を効率よく認識して攻撃できるようにする治療法。 |
|
(注11) |
CAR-T |
がん免疫療法の一種であり、T細胞がCAR(キメラ抗原受容体)と呼ばれる特殊なたんぱく質を作り出せるように遺伝子を改変することで、改変されたT細胞が、がん細胞を効率よく認識して攻撃できるようにする治療法。 |
|
(注12) |
AI創薬 |
AI(人工知能)技術を活用することで、医薬品候補分子の探索や薬剤の効果や副作用を予測するなど、創薬プロセスを大幅に短縮すると同時に、医薬品開発の成功確率の改善を目指す手法。 |
当社では、がんや自己免疫疾患、感染症やアレルギーなどの様々な種類の病気に免疫系が関与していることに着目し、また人が過去から現在までに遭遇した病気の記憶は、免疫系内に保存されていることから、この免疫系の包括的で詳細な理解が、病気の原因や薬の作用メカニズムの解明に欠かせないものであり、免疫系の多様性解析を活用することで、これまでにない画期的な予防、診断、治療法を開発することが可能となると考えております。中長期的には、免疫多様性情報に基づいた治療法の選択や個別化医療を実現することが、世界中で今後加速すると考えられる免疫関連疾患の増大と医療経済のひっ迫という大きな社会課題を解決し、当社のミッションである「治らないをなくす」ことの実現につながると考えております。
② 当社技術の特長
免疫系の詳細な理解に基づいて、新しい治療法や診断法を開発する試みは、当社の創業以前にもありましたが、その実現は容易ではありませんでした。その理由としては、免疫系が数多くの外来性の抗原(注13)に対応するために元々備えている多様性の規模が大きいため、正確にその全貌を把握することが困難であったためです。そこで、当社は、免疫系の多様性と特異性についての把握に必須となる次世代型のTCR/BCRレパトア解析を開発しました。
<用語解説>
|
(注13) |
抗原 |
生体内で抗体を形成させる物質のこと。抗体は抗原と特異的に結合し、その異物を生体内から除去する物質のこと。 |
a.TCR/BCRレパトア解析
生体には体外から侵入した細菌やウイルス等の病原体から生体を防御する免疫系が備わっています。免疫系において重要な働きを担っているのが、リンパ球に含まれるT細胞とB細胞です。これらの細胞は、細胞表面にあるT細胞受容体(TCR)やB細胞受容体(BCR)という受容体分子によって、様々な病原体の持つ抗原を認識して攻撃するだけでなく、がん細胞などの体内で生じた異常な細胞を見つけ出し排除する役割も担っています。そのためT細胞やB細胞は、一つ一つの細胞の表面に異なる受容体分子を持っており、その受容体の種類に応じて異なる抗原を認識することができる仕組みとなっております。
TCR/BCRレパトア解析は、これら一つ一つのT細胞とB細胞が持つ受容体の遺伝子を網羅的に解析することで、個々のT細胞やB細胞がどのような抗原に反応しているのか(特異性)や、どれくらいの種類の受容体を全体として持っているのか(多様性)を明らかにするものです。
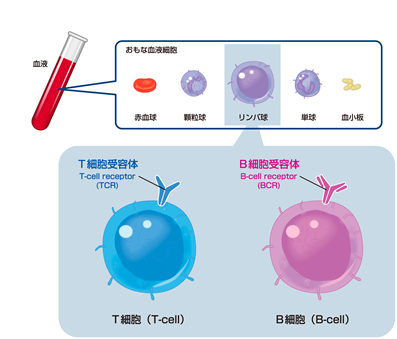
<血液におけるT細胞とB細胞の位置づけ>
リンパ球は血液細胞の一部で、さらにT細胞、B細胞などに分類される
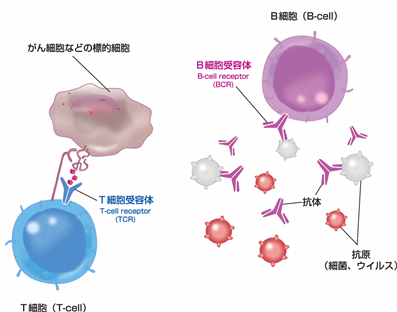
<T細胞受容体(TCR)とB細胞受容体(BCR)>
T細胞受容体とB細胞受容体が標的物質を認識
b.TCR/BCRレパトア解析の有用性
TCR/BCRレパトア解析は、我が国の科学技術イノベーション政策に関する調査、分析、提案を中立的な立場で行うJST研究開発戦略センター(CRDS)による2019年の報告書の中でも、「今後重要になると考えられる重要研究・技術開発テーマ群」に位置づけられているように※2、近年注目度が高まってきている技術です。特に、病気の原因や、免疫系と病気との関連を調べ、治療によって患者さんの免疫状態がどのように変化するかを、T細胞やB細胞の特異性や多様性から明らかにすることができ、具体的には以下のような医療開発の場面で活用されています。
※2:出典 国立研究開発法人科学技術振興機構 研究開発戦略センター 俯瞰ワークショップ報告書「次世代医薬・基盤技術の動向と展望、推進すべき研究開発戦略」(CRDS-FY2018-WR-12)
(ア)がん免疫療法の有効性評価、バイオマーカー開発
がん治療の分野では、近年免疫系を利用した治療法(がん免疫療法)の開発が盛んに行われています。これら治療法の多くは、患者さん自身のT細胞やB細胞の働きを利用しています。TCR/BCRレパトア解析は、がん組織、あるいは血液中に存在する免疫細胞が治療によってどのように変化するかを明らかにすることができ、がん免疫療法の有効性や安全性の評価に利用することができます。特に免疫チェックポイント阻害薬は高い治療効果が示されているがん免疫治療薬であり、現在も様々な種類の免疫チェックポイント阻害薬の開発が世界中の製薬企業によって進められています。これらの薬は一部のがん種や症状に対して有効ではありますが、効果のある患者さんは限られ、有効な患者さんを予測するバイオマーカーの開発が求められています。免疫チェックポイント阻害薬の効果は患者さんの免疫状態に影響を受ける可能性があり、TCR/BCRレパトア解析から得られる情報が有用なバイオマーカーの開発につながると期待されます。
(イ)免疫療法の開発
TCR/BCRレパトア解析を用いて、特定の抗原で刺激する前後の検体サンプルを比較することで、抗原刺激によって増加した免疫細胞を探索することができ、また抗原刺激によって誘導されたT細胞やB細胞が持っているTCR/BCR遺伝子の配列を決定することができます。抗原に反応するTCR/BCRの遺伝子配列を特定できれば、そのTCR/BCR遺伝子を人為的に免疫細胞に導入することで遺伝子改変型の細胞療法を実現することや抗体医薬の開発につなげることができます。
(ウ)自己免疫疾患のバイオマーカー
関節リウマチなどの自己免疫疾患は、本来は異物を認識し排除する役割を持つ免疫系が、正常な細胞や組織に対して過剰に反応してしまうことで起こる病気です。多くの自己免疫疾患の原因は十分に明らかにされておらず、様々な免疫系の異常により発症すると考えられています。TCR/BCRレパトア解析により、自己免疫疾患に特徴的なT細胞やB細胞の異常が明らかになれば、それらをバイオマーカーとして利用することができます。また、T細胞の異常に起因する患者さんや、抗体を産生するB細胞の異常が原因となる患者さんが分かれば、それらの患者さんに対するより効果的な治療法の開発が可能になります。
(エ)ワクチンの作用機序の解明
TCR/BCRレパトア解析はワクチン開発にも有用です。ワクチン投与後に、T細胞やB細胞がどのような変化を示すのかをTCR/BCRレパトア解析により明らかにすることができます。抗原に特異的なT細胞が誘導される様子や抗体を産生するB細胞を検出できるので、ワクチンがどのような作用機序で働くのかを調べることが可能になり、より効果的なワクチンの開発が可能になります。
c.当社技術の優位性
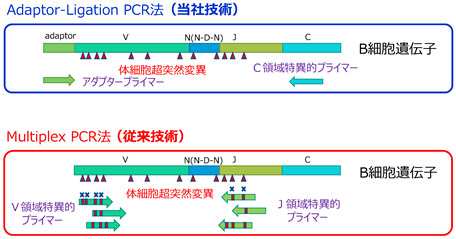
TCR/BCR遺伝子は、多数のV領域、D領域及びJ領域(注14)の遺伝子断片の組み合わせによって、多くの種類の遺伝子配列が作りだされます。そのため、これら遺伝子をPCR(注15)によって増幅するためには、V領域とJ領域それぞれに数十種類を超える多数のプライマー(注16)を用いて増幅するMultiplex PCR法が一般的には用いられます。このMultiplex PCR法を用いた場合、プライマー間の遺伝子増幅効率の差により、PCR増幅反応の過程でバイアス(偏り)が生じ、正確性を欠く結果になります。
そこで当社では、1セットのアダプタープライマーとC領域に特異的なプライマーを用いて増幅するAdaptor-ligation PCR法を開発し、2017年に特許を取得いたしました(特許第6164759号)。当社が開発したAdaptor-ligation PCR法では、異なるV領域やJ領域を持つ全てのTCR/BCR遺伝子を、1セットのプライマーで増幅することが可能であり、Multiplex PCR法で問題となる解析データの偏りが起こりません。また、B細胞は抗原との結合力を増すためにV領域、J領域の遺伝子配列に体細胞超突然変異が発生することが知られていますが、当社の増幅手法ではプライマーの結合に影響を受けることがないため、正確性の高い遺伝子増幅が可能となります。
<当社技術の特長>
異なるV領域やJ領域を持つ全てのTCR/BCR遺伝子を、1セットのプライマーで増幅することで高精度な解析を実現
この結果、当社の解析の結果は、特に高い信頼性が要求される新規の予防、診断、治療法の開発に適しています。
以上の当社のTCR/BCRレパトア解析の特長をまとめると、以下のとおりとなります。
|
|
一般的な解析手法 (Multiplex PCR法) |
当社の解析手法 (Adaptor-ligation PCR法) |
|
使用するプライマー |
複数セット(数十セット超) |
1セット |
|
解析データの偏り |
発生する |
発生しない |
<用語解説>
|
(注14) |
V領域、D領域、J領域 |
TCR及びBCRの構成遺伝子のこと。ゲノム上では多数のV(variable)、D(diversity)、J(joining)及びC(constant)の遺伝子断片からなり、T/B細胞の成熟の過程で遺伝子再構成が行われ、これらの遺伝子の組み合わせによって大きな多様性が生み出される。 |
|
(注15) |
PCR |
Polymerase Chain Reaction(ポリメラーゼ連鎖反応)の略で、DNAの特定の部位だけを増幅する方法のこと。 |
|
(注16) |
プライマー |
目的の遺伝子を増幅するために用いる人工的に作られた成分のこと。 |
d.当社技術の広がり
免疫系の解明及び新規の予防、診断、治療法の開発には、TCR/BCRレパトア解析以外にも、様々な技術が必要となるため、当社では免疫多様性解析に関する一連の関連技術群の開発を進めております。一例としては、がん細胞などの病気の細胞のみに存在している、正常な細胞とは異なる変異ペプチド(ネオエピトープ)を正確に判定するネオエピトープ解析技術を保有しております。
<ネオエピトープ解析>
病気の細胞のみに存在している変異ペプチド(ネオエピトープ)を正確に判定
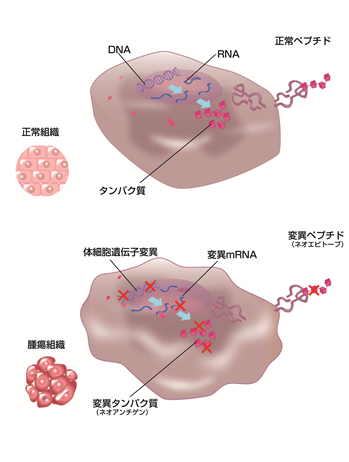
従来型のネオエピトープ解析では、遺伝子上の1ヶ所のアミノ酸変異によってネオエピトープが発生した場合にしか解析することができませんでした。しかしながら実際には、そのような場合だけでなく、遺伝子に構造上の変化が生じた場合にも、ネオエピトープが発生することがあります。そこで、当社では、独自の解析アルゴリズムを駆使することで、従来型ネオエピトープ解析では解析することができなかった、遺伝子に構造上の変化があった場合も対応可能な解析系を構築し2020年に特許を取得いたしました(特許第6710004号)。そのため、当社の解析結果は、特に高い信頼性が要求される新規の予防、診断、治療法の開発に適しています。
以上の当社のネオエピトープ解析の特長をまとめると、以下のとおりとなります。
|
|
従来のネオエピトープ解析 |
当社のネオエピトープ解析 |
|
1ヶ所のアミノ酸変異 |
検出可能 |
検出可能 |
|
遺伝子の構造変化 |
検出不可能 |
検出可能 |
また、当社ではシングルセル解析(注17)とTCR/BCRレパトア解析を組み合わせることで、免疫応答の原因となっているT細胞、B細胞を1細胞単位で決定し、またそのTCR/BCR配列を取得し、さらにゲノム編集技術と遺伝子導入技術を活用した細胞療法の開発に取り組む※3などの応用的な研究開発も推進しております。
※3:国立研究開発法人日本医療開発研究機構(AMED)採択課題:NY-ESO-1 特異的高機能ゲノム編集T細胞の製造基盤技術の確立
<用語解説>
|
(注17) |
シングルセル解析 |
シングルセル(単一細胞)単位でDNAの状態やメッセンジャーRNAの発現量などを解析する手法。 |
(2) 当社のビジネスモデル
当社は、顧客の医療開発に対して、免疫系を応用した新規医療開発支援事業を単一セグメントで展開しているため、セグメント別の記載は行っておりませんが、開発支援サービスの提供方法の違いにより「研究開発支援」及び「臨床開発支援」と2つの売上区分を定義しております。
<医薬品の開発工程と当社開発支援サービスとの関係>
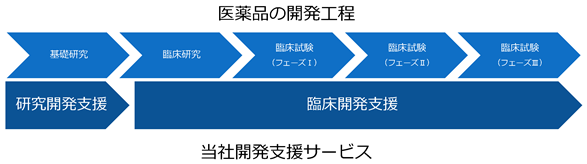
「研究開発支援」とは、顧客の基礎的な研究開発を支援する区分であり、主に大学や公的な研究機関などのアカデミアを対象とした比較的小規模な研究支援サービスを主に販売代理店経由で顧客に提供する事業領域を言います。
「臨床開発支援」とは、顧客の応用的な臨床開発を支援する区分であり、主に製薬企業を対象として臨床サンプルを利用した比較的大規模で長期間にわたる開発プロジェクトを推進する事業領域です。
<事業系統図>
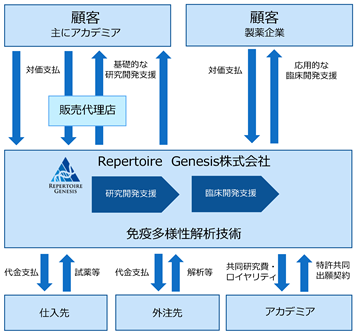
① 研究開発支援
「研究開発支援」においては、主要顧客である大学・公的研究機関等のアカデミアに対して、当社独自の免疫多様性解析サービスを販売代理店経由で提供しております。
主要サービスとして、TCR/BCRレパトア解析があり、顧客における当社技術の利用目的は多岐にわたっておりますが、様々な疾患の基礎的な免疫メカニズムの解明や新規の予防、診断、治療法の初期的な探索などが代表的なものとなります。
研究開発支援における基本的な課金体系としては、解析量に応じた従量課金方式となり、比較的金額は小さく、かつ単発的な収益となりますが、安定的な売上に貢献するのみならず、最先端の研究をされているアカデミアのKOL(キーオピニオンリーダー)などの専門家との積極的な意見交換や共同研究に基づいた技術の開発・特許の共同出願を推進することで、当社の中長期的な発展の礎とするオープンイノベーション的な要素も企図した事業領域となります。
② 臨床開発支援
「臨床開発支援」においては、主要顧客である製薬企業等と開発内容と経済条件をよく協議したうえで、直接契約をし、当社の免疫多様性解析技術・ノウハウ・情報等と製薬企業の新規医薬品候補・既存医薬品・ノウハウ・情報等とを連携することで、これまでにない新しい予防、診断、治療法を開発しております。
臨床開発支援における基本的な課金体系としては、プロジェクト規模に応じた複数年契約を基本とした従量課金方式となり、比較的金額は大きく、かつ中長期的な収益貢献となります。尚、リスクとリターンのバランスに応じてプロジェクトから得られた成果物が共有となり、将来の売上ロイヤリティが生じる共同研究開発形式の契約となることもあります。
<臨床開発支援におけるプロジェクトと契約条件事例(2021年12月時点*1)>
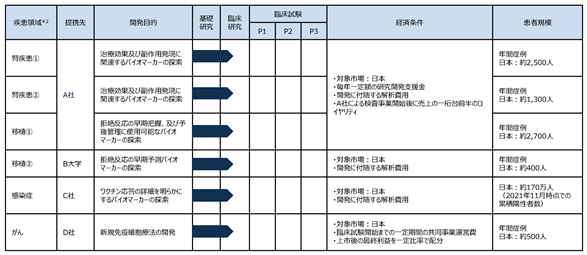
*1 上記以外にも2021年12月期において、4本の臨床開発支援プロジェクトの稼働実績があります。
*2 具体的な適応疾患名は提携先との契約上で原則非開示とされているため記載しておりません。
<売上区分の比較説明>
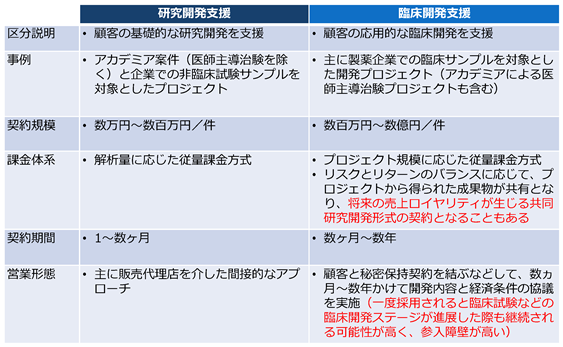
③ 研究開発支援と臨床開発支援の関係性
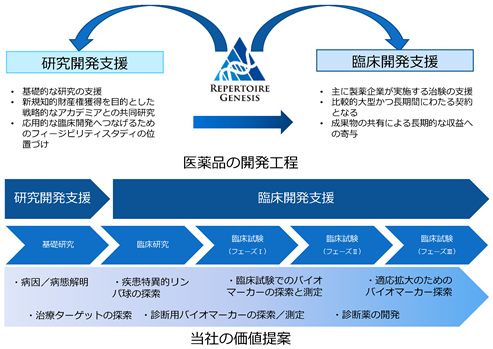
上図は、医薬品の各開発工程において、当社が顧客に提案する価値類型を示したものです。医薬品開発の上流から下流までをシームレスに幅広く価値提案することで安定的な収益基盤の構築と高い成長可能性の両立を実現する安定的高成長モデルとなっていると考えております。
当社では、主にアカデミアの基礎的な研究ニーズに応える形で、独自性の高い研究開発支援サービスを提供することで、顧客が新規性の高い研究成果が出せるように支援しております。また、基礎的な研究で一定の評価が得られた場合には、アカデミアの基礎研究からヒトの臨床サンプルを利用した臨床開発に開発フェーズが移行しますが、当社では臨床開発のニーズに対応するために、2018年7月に医薬品の安全性に関する非臨床試験の実施の基準に関する省令(医薬品GLP省令)に準じて当社の開発した解析サービスを提供する体制を構築しました。さらに2019年3月にはレパトア解析の分野でISO/IEC 17025:2017(注18)の認定を取得したことによって、当社の独自性の高い解析に対して国際的な信頼性が付与されたと考えており、製薬企業との長期的な臨床開発案件の増大につながっております。
<用語解説>
|
(注18) |
ISO/IEC 17025:2017 |
「ISO/IEC 17025:2017」は、スイスのジュネーブに在る国際標準化機構が策定している国家間に共通な標準規格のうちの一つ。特定の種類の試験及び校正を実施する試験所の技術能力を証明するもので、ISO9001で要求される品質マネジメントに関する要件に加えて、試験を正しく実施する技術力があることが要求されている。 |
(3) 当社の成長戦略
世界で拡大を続けている免疫系を応用した医療開発ニーズを確実に捉えていくために、3本の成長軸を基本とした成長戦略を遂行しております。具体的には、①基礎的な研究開発支援から応用的な臨床開発支援へと開発フェーズをステップアップさせるという事業軸、②同一製薬企業内でも複数本の開発案件に提携を広げるプロジェクト展開軸、③国内外の顧客数を増やす顧客軸、という3本の成長軸で、今後も金額規模が大きく契約期間の長い臨床開発支援案件を多く獲得することにより、安定的かつ高い成長性の実現を目指します。
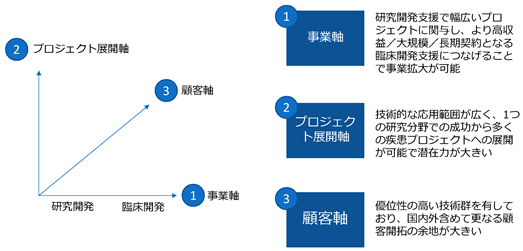
① 事業軸:臨床開発支援の拡大
当社は、免疫の多様性解析があまり脚光を浴びていなかった頃から、富士フイルム和光純薬株式会社(富士フイルムグループ)との間で受託サービス仲介契約を締結し、同社の日本全国を網羅するきめ細やかな販売ネットワークを通じて、大学と研究機関を中心に事業活動を続けてきました。また、当社は免疫多様性解析のパイオニアとして培われた経験・事例・ノウハウを活かして、顧客ごとの異なる研究課題や開発目的に応じた適切な研究提案やサービスを提供していることから、アカデミアの先進的な研究をされている研究者達との幅広いネットワークを築いており、がん免疫療法の効果予測マーカーや自己免疫系神経疾患の血液診断法など、今後の事業成長に資する知的財産権につき当該研究者と共同出願する機会を有しています。
この結果、単に顧客数を増加させるという営業戦略のみならず、アカデミアにおいては研究的要素が強く新規性の高い共同研究を戦略的に増加させることに伴い、臨床開発の主体となる製薬企業に訴求できる知的財産やノウハウを蓄積するといった事業戦略を取っております。
つまり、当社の免疫多様性解析技術は、研究開発支援における関与プロジェクト数の増加に伴って知的財産権やノウハウの蓄積が増加することにより有用性が高まり、その効果を一つのターゲット(上記の例では、研究開発支援を中心とした顧客の集合)だけでなく、他のターゲット(上記の例では、臨床開発支援を中心とした顧客の集合)においても多面的に享受することが可能となっています。そのため、当社の免疫多様性解析技術は、研究開発支援における関与プロジェクト数の増加により新たなサービス・製品が創出され、新たに創出されたサービス・製品が臨床開発支援における新たな顧客の呼び水になるという好循環を生んでおります。
これらのことから、当社は、単に解析技術(要素技術)が優れているのみならず、その技術の活用イメージの提案力、今までのサービス提供で培われた経験・事例・ノウハウ・ネットワーク、信頼性、実証実験を通じて技術を確立する開発力といった、単に解析にとどまらない能力を有しており、アカデミアとの研究開発案件を製薬会社との大型の臨床開発へと移行させるという事業軸を意識した活動を行っております。
② プロジェクト展開軸:1つの研究分野での成功を起点とした複数プロジェクトへの拡大
当社の技術は、技術的な応用範囲が広く、1つの研究分野での成功から多くの疾患プロジェクトへの展開が可能であり潜在力が大きいことが特長です。あるアカデミアとの共同研究の成果を元にして、臨床開発支援がスタートした製薬企業とのプロジェクトが大幅に増えたケースもあります。今後も同一企業内の多くの創薬プロジェクトにおいて当社技術を広める活動を推進していきます。
<研究開発支援から臨床開発支援への拡がり>
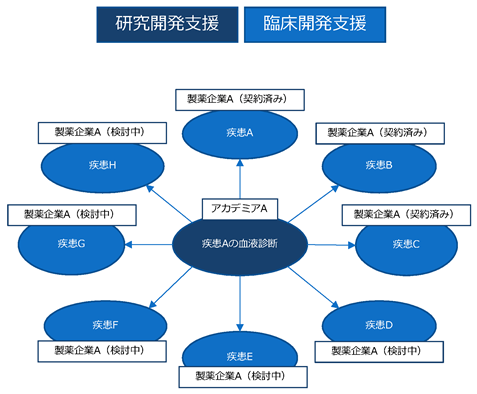
③ 顧客軸:優位性の高い技術群を活かし国内外の顧客を拡大
TCR/BCRレパトア解析は製薬企業等の治験や臨床試験において活用されており、高い信頼性が求められます。解析の信頼性を担保するため、当社は、医薬品GLP省令の基準に従って、TCR/BCRレパトア解析を提供する体制を構築しております。これにより当社は、信頼性の高い解析サービスを製薬企業等の治験や臨床試験に提供することが可能な体制を整えております。また、2019年3月19日には、当社研究所が日本適合性認定協会から、TCR/BCRレパトア解析を対象として国際規格「ISO/IEC 17025:2017」を取得いたしました。当該規格は特定の種類の試験及び校正を実施する試験所の技術能力を証明するものであり、この認定により、当社研究所の技術能力が国際標準規格に適合していることが証明され、顧客に質の高いサービスを提供していることが客観的に示されたと当社では考えております。
当社は、国内で多くのアカデミアと製薬企業に当社技術を採用していただいているという実績を武器としながら、技術能力の観点からも当社が国際標準規格に適合していることを強みとして、国内外の幅広い顧客からの新規採用を増やすべく業務に取り組んでおります。
4【関係会社の状況】
該当事項はありません。
5【従業員の状況】
(1)提出会社の状況
|
|
|
|
|
2021年12月31日現在 |
|
従業員数(人) |
平均年齢(歳) |
平均勤続年数(年) |
平均年間給与(円) |
|
|
|
( |
|
|
|
(注)1.臨時雇用者数(パートタイマーを含む。)は、最近1年間の平均人員を( )外数で記載しております。
2.平均年間給与は、賞与及び基準外賃金を含んでおります。
3.当社の報告セグメントは免疫系を応用した新規医療開発支援事業の単一セグメントであるため、セグメント別の従業員数については、記載を省略しております。
(2)労働組合の状況
当社において労働組合は、結成されておりませんが、労使関係は円満に推移しております。