第二部【企業情報】
第1【企業の概況】
1【主要な経営指標等の推移】
|
回次 |
第9期 |
第10期 |
第11期 |
第12期 |
第13期 |
|
|
決算年月 |
2015年12月 |
2016年12月 |
2018年3月 |
2019年3月 |
2020年3月 |
|
|
売上高 |
(千円) |
|
|
|
|
|
|
経常利益又は経常損失(△) |
(千円) |
|
△ |
△ |
△ |
△ |
|
当期純利益又は当期純損失(△) |
(千円) |
|
△ |
△ |
△ |
△ |
|
持分法を適用した場合の投資利益 |
(千円) |
|
|
|
|
|
|
資本金 |
(千円) |
|
|
|
|
|
|
発行済株式総数 |
(株) |
|
|
|
|
|
|
普通株式 |
|
|
|
|
|
|
|
A種優先株式 |
|
|
|
|
|
|
|
純資産額 |
(千円) |
|
|
|
|
|
|
総資産額 |
(千円) |
|
|
|
|
|
|
1株当たり純資産額 |
(円) |
|
|
△ |
△ |
|
|
1株当たり配当額 |
(円) |
|
|
|
|
|
|
(うち1株当たり中間配当額) |
( |
( |
( |
( |
( |
|
|
1株当たり当期純利益又は 1株当たり当期純損失(△) |
(円) |
|
△ |
△ |
△ |
△ |
|
潜在株式調整後1株当たり 当期純利益 |
(円) |
|
|
|
|
|
|
自己資本比率 |
(%) |
|
|
|
|
|
|
自己資本利益率 |
(%) |
|
|
|
|
|
|
株価収益率 |
(倍) |
|
|
|
|
|
|
配当性向 |
(%) |
|
|
|
|
|
|
営業活動によるキャッシュ・フロー |
(千円) |
|
|
|
△ |
△ |
|
投資活動によるキャッシュ・フロー |
(千円) |
|
|
|
△ |
|
|
財務活動によるキャッシュ・フロー |
(千円) |
|
|
|
|
△ |
|
現金及び現金同等物の期末残高 |
(千円) |
|
|
|
|
|
|
従業員数 |
(人) |
|
|
|
|
|
|
(外、平均臨時雇用者数) |
( |
( |
( |
( |
( |
|
(注)1.当社は連結財務諸表を作成しておりませんので、連結会計年度に係る主要な経営指標等の推移については記載しておりません。
2.2017年12月22日開催の臨時株主総会決議により、決算期を12月31日から3月31日に変更いたしました。これに伴い、第11期は2017年1月1日から2018年3月31日までの15ヶ月間となっております。
3.売上高には、消費税等は含まれておりません。
4.持分法を適用した場合の投資利益については、当社は関連会社を有していないため、記載しておりません。
5.1株当たり配当額については、配当を実施していないため、記載しておりません。
6.第9期の潜在株式調整後1株当たり当期純利益については、潜在株式が存在しないため、記載しておりません。
第10期、第11期、第12期及び第13期の潜在株式調整後1株当たり当期純利益については、潜在株式は存在するものの、当社株式は非上場であり、期中平均株価を把握できないため、また、1株当たり当期純損失であるため、記載しておりません。
7.第10期、第11期、第12期及び第13期の自己資本利益率については、当期純損失であるため、記載しておりません。
8.株価収益率については、当社株式は非上場であるため、記載しておりません。
9.配当性向については、配当を実施していないため、記載しておりません。
10.第11期まではキャッシュ・フロー計算書を作成しておりませんので、キャッシュ・フローに係る項目については記載しておりません。
11.従業員数は、就業人員であり、臨時雇用者数は、1年間の平均人員を( )内に外数で記載しております。
12.第12期及び第13期の財務諸表については、「財務諸表等の用語、様式及び作成方法に関する規則」(1963年大蔵省令第59号)に基づき作成しており、金融商品取引法第193条の2第1項の規定に基づき、EY新日本有限責任監査法人の監査を受けております。
なお、第9期、第10期及び第11期については、「会社計算規則」(2006年法務省令第13号)の規定に基づき算出した各数値を記載しております。また、当該各数値については、金融商品取引法第193条の2第1項の規定に基づくEY新日本有限責任監査法人の監査を受けておりません。
13.当社は、2019年11月14日付で普通株式及びA種優先株式それぞれ1株につき100株の割合で株式分割を行っております。第12期の期首に当該株式分割が行われたと仮定し、1株当たり純資産額及び1株当たり当期純損失を算定しております。
14.当社は、2019年11月14日付で普通株式及びA種優先株式それぞれ1株につき100株の割合で株式分割を行っております。
そこで、東京証券取引所自主規制法人(現 日本取引所自主規制法人)の引受担当者宛通知「『新規上場申請のための有価証券報告書(Ⅰの部)』の作成上の留意点について」(2012年8月21日付東証上審第133号)に基づき、第9期の期首に当該株式分割が行われたと仮定して算出した場合の1株当たり指標の推移を参考までに掲げると、以下のとおりとなります。
なお、第9期、第10期及び第11期の数値(1株当たり配当額についてはすべての数値)については、EY新日本有限責任監査法人の監査を受けておりません。
|
回次 |
第9期 |
第10期 |
第11期 |
第12期 |
第13期 |
|
|
決算年月 |
2015年12月 |
2016年12月 |
2018年3月 |
2019年3月 |
2020年3月 |
|
|
1株当たり純資産額 |
(円) |
1,321.32 |
5.09 |
△76.29 |
△142.57 |
34.57 |
|
1株当たり当期純利益又は 1株当たり当期純損失(△) |
(円) |
97.10 |
△29.64 |
△81.38 |
△66.28 |
△61.68 |
|
潜在株式調整後1株当たり 当期純利益 |
(円) |
― |
― |
― |
― |
― |
|
1株当たり配当額 |
(円) |
― |
― |
― |
― |
― |
|
(うち1株当たり中間配当額) |
(―) |
(―) |
(―) |
(―) |
(―) |
|
2【沿革】
当社が開発を進めるホウ素中性子捕捉療法(以下「BNCT※」という。)は、中性子が発見された4年後の1936年には理論上は考案されていた治療法ですが、実現には、患部に高い選択性で集積し、かつ効果的な反応が得られるホウ素薬剤と高強度の中性子源が必要不可欠であり、永らく実用化が困難とされた治療法でした。
当社の代表取締役会長である浅野智之は、ステラケミファ株式会社在籍時に同社が持つホウ素同位体の高濃縮技術に着目し、がん治療におけるBNCTの活用に向けて、より効果的なホウ素薬剤の開発を進めてまいりました。また、高強度の中性子発生装置についても、従来は医療現場への設置が不可能な原子炉のみでしたが、住友重機械工業株式会社において、BNCTに適した中性子線を発生させる小型の加速器が開発されました。これによりBNCTの実用化における最大の障壁となっていた「効果的なホウ素薬剤」と医療現場への設置が可能な「高強度の中性子源」の2つの要件が揃ったことから、BNCTの事業化を目的にステラケミファ株式会社の子会社として当社は設立されました。
※BNCT……Boron Neutron Capture Therapyの略称。
BNCTとは、放射線治療の一種であり、新しいがんの治療法です。ホウ素の安定同位体であるB-10(天然ホウ素に約20%含まれる)の原子核はエネルギーの低い低速の中性子(熱中性子)をよく吸収し、直ちにヘリウム原子核(4He核(α粒子))とリチウム原子核(7Li核)に分裂します。これら原子核は細胞を破壊する能力が非常に大きい一方で、影響を及ぼす範囲が4~9ミクロン(μm)と極めて短いことが特徴です。また、熱中性子自体の細胞破壊能力は小さいため、B-10を含む物質ががん細胞に選択的に集積し、そこに熱中性子が照射されると、そのがん細胞は選択的に破壊されます。この原理に基づいて考案された医療技術がBNCTです。
以降、本書提出日現在までの主な変遷は次のとおりであります。
|
年月 |
事業の変遷 |
|
2007年6月 |
ステラケミファ株式会社(大阪市中央区)の100%子会社として法人設立 |
|
2008年7月 |
第一種医薬品製造販売業許可を取得(大阪府) |
|
2009年1月 |
開発品SPM-011が、独立行政法人科学技術振興機構(現 国立研究開発法人科学技術振興機構)が支援する独創的シーズ展開事業の委託開発課題に採択 (現在は国立研究開発法人 日本医療研究開発機構が実施する医療分野研究成果展開事業に移管) |
|
2012年11月 |
開発品SPM-011の日本における脳腫瘍 第Ⅰ相臨床試験を開始 (脳腫瘍の対象は、再発悪性神経膠腫患者) |
|
2013年12月 |
第一種医療機器製造販売業許可を取得(大阪府) |
|
2014年1月 |
研究開発業務の効率化を目的として、公立大学法人大阪府立大学(現 公立大学法人大阪)BNCT研究センター内に研究所(さかい創薬研究センター)を移設(堺市中区) |
|
2014年4月 |
開発品SPM-011の日本における頭頸部癌 第Ⅰ相臨床試験を開始 (頭頸部癌の対象は、切除不能な局所再発頭頸部癌及び切除不能な局所進行頭頸部癌(非扁平上皮癌)患者) |
|
2016年2月 |
開発品SPM-011の日本における脳腫瘍 第Ⅱ相臨床試験を開始 (脳腫瘍の対象は、再発悪性神経膠腫患者) |
|
2016年3月 |
株式会社産業革新機構(現 株式会社INCJ)及び住友重機械工業株式会社を引受先として、第三者割当の方法により増資を実施 (ステラケミファ株式会社の議決権保有割合は63.9%に減少) |
|
2016年7月 |
開発品SPM-011の日本における頭頸部癌 第Ⅱ相臨床試験を開始 (頭頸部癌の対象は、切除不能な局所再発頭頸部癌及び切除不能な局所進行頭頸部癌(非扁平上皮癌)患者) |
|
年月 |
事業の変遷 |
|
2017年4月 |
開発品SPM-011が、厚生労働省が実施する先駆け審査指定制度の対象品目(医薬品)として指定 |
|
2018年5月 |
東京事務所を開設(東京都中央区) |
|
2019年11月 |
開発品SPM-011の日本における悪性黒色腫及び血管肉腫 第Ⅰ相臨床試験を開始 |
|
2020年3月 |
日本において、切除不能な局所進行又は局所再発の頭頸部癌を効能・効果として、BNCT用ホウ素薬剤ステボロニン®点滴静注バッグ 9000 mg/300 mL(一般名:ボロファラン(10B)、開発品名:SPM-011 以下、「ステボロニン®」という)の製造販売承認を取得 |
|
2020年5月 |
ステボロニン®の販売を開始 |
|
2020年10月 |
株式会社スズケン及び株式会社ハイメディックを引受先として、第三者割当の方法により増資を実施 (ステラケミファ株式会社の議決権保有割合は63.4%に減少) |
3【事業の内容】
当社は、企業理念として『ひとりのかけがえのない命のために、ステラファーマは世界の医療に新たな光を照らします。』を掲げ、「ひとりのかけがえのない命のために」それぞれの使命を実行することを行動指針の基盤とし、「世界の医療に新しい光を照らす」ことを経営目標の策定方針としております。
当社は、この企業理念に基づき、がん患者に対する新たな治療の選択肢としてBNCTを実用化するため、創業以来、BNCT用ホウ素薬剤の研究及び開発に取り組んでまいりました。
(1)事業の特徴
①BNCTの医療技術
BNCTは、ホウ素の安定同位体であるB-10とエネルギーの小さな熱中性子の核分裂反応を利用して、がん細胞を選択的に破壊する放射線治療の一手法であります。
ホウ素の安定同位体であるB-10(天然ホウ素に約20%含まれる)の原子核はエネルギーの低い低速の中性子(熱中性子)をよく吸収し、直ちにヘリウム原子核(4He核(α粒子))とリチウム原子核(7Li核)に分裂します。これら原子核は細胞を破壊する能力が非常に大きい一方で、影響を及ぼす範囲が4~9ミクロン(μm)と極めて短く、また、熱中性子自体の細胞破壊能力は小さいため、B-10を含む物質が、がん細胞に選択的に集積し、そこに熱中性子が照射されると、そのがん細胞は選択的に破壊されます。この原理に基づいて考案された医療技術がBNCTであります。
[BNCTの治療イメージ]
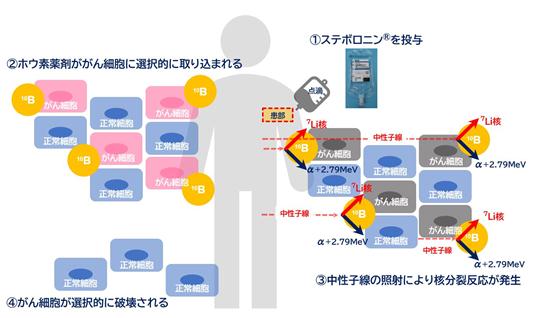
BNCTは、その特徴として、『がん細胞を選択的に破壊』することができる治療法であることから、がん細胞と入り組む正常組織への影響が少なく、術後のQOL(Quality Of Life/生活の質)も従来の治療に比べて良好であることが期待されます。
②ビジネスモデルについて
当社が、2020年3月に、切除不能な局所進行又は局所再発の頭頸部癌を効能・効果として、ステボロニン®の医薬品製造販売承認を取得したことに伴い、既に加速器を設置しております総合南東北病院、大阪医科大学附属病院の2つの医療施設においてBNCTによる治療が開始されております。当社は国内において治療が開始されたことに伴い、医薬品卸売業者を介した自販モデルによる収益化を実現しております。
今後も加速器メーカーとの共同でステボロニン®の適応拡大に向けた研究開発及び臨床試験を継続していくと同時に、当社の製品は加速器メーカーとのコンビネーションプロダクトをベースとしていることから、BNCTの認知度向上と加速器の普及に向けた事業展開も並行的に進めることで、収益拡大を実現していくビジネスモデルであります。
(2)開発品の特徴
①開発品の概要について
当社が、開発、製造及び販売するステボロニン®(開発品名:SPM-011)は、厚生労働省の実施する先駆け審査指定制度の対象品目に指定されており、2020年3月にBNCT用ホウ素薬剤として世界初となる薬事承認を取得しております。
BNCTは、その性質上、中性子の発生装置となる医療機器と医薬品を組み合わせた治療法であり、患部に高い選択性で集積し、かつ効果的な反応が得られるホウ素薬剤が必要となります。
[ステボロニン®点滴静注バッグ 9000 mg/300 mL]

②開発品の作用機序について
天然ホウ素には、中性子数の異なるホウ素10(B-10)とホウ素11(B-11)の2種類が存在し、B-10は約20%の割合で存在しています。BNCTにおいて核分裂反応を起こすホウ素はB-10のみであるため、効果的なホウ素薬剤とするためには、B-10を高純度に濃縮し、より多く含有する製剤を作る必要があります。
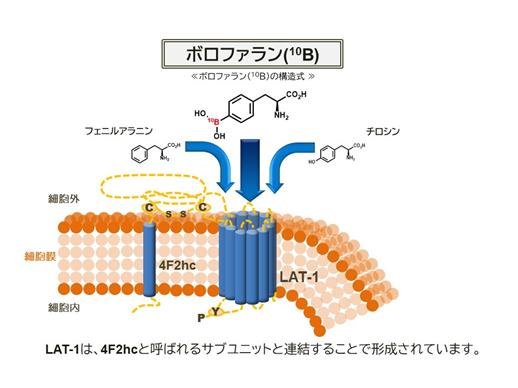
当社の開発品であるステボロニン®は、この高純度(99%以上)B-10を含む「ボロファラン(10B)※1」を原薬として製造しております。ボロファラン(10B)は、必須アミノ酸であるフェニルアラニン※2又はチロシン※3と構造が似ているため、がん細胞特有のアミノ酸トランスポーターであるLAT-1※4を介してアミノ酸要求性の高いがん細胞に取り込まれます。これにより、がん細胞に選択的にB-10が集積し、かつ中性子線を照射した際により大きな効果を得ることが可能となります。
[ボロファラン(10B)の構造式とがん細胞への取込みの作用機序]
③開発品の競争優位性について
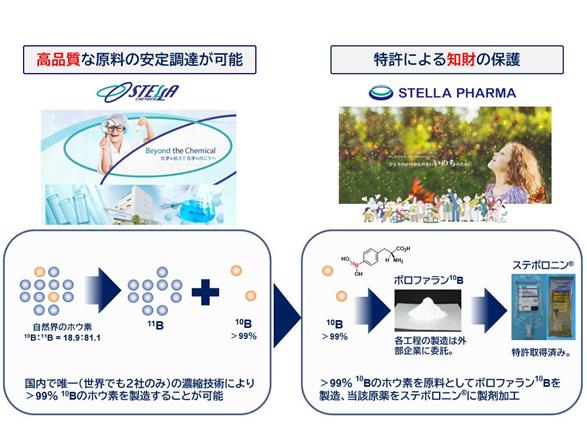
B-10を高純度(99%以上)に濃縮する技術は、当社の親会社であるステラケミファ株式会社が国内で唯一(世界でも2社のみ)保有しているものと認識しております。
当社は、高純度(99%以上)まで濃縮されたB-10を原料として、原薬「ボロファラン(10B)」を製造し、さらにステボロニン®に製剤加工しております。原料については親会社であるステラケミファ株式会社との間で独占期間を定めた取引基本契約を締結し、安定的に原料供給を受ける調達体制をとっております。また製剤処方にかかる特許権を複数取得しており、今後も周辺特許の申請を積極的に行っていく方針であります。ステボロニン®は臨床研究において従来使用されていたフルクトース製剤に比べ安定性に優れ、さらに36ヶ月という長期の品質有効期間を保ち、治療毎に製剤を調製する必要もなく、また「医薬品の製造管理及び品質管理の基準(GMPgrade)」に適合した製剤でもあります。
この特徴に加え、当社における長年の研究開発期間と相当程度の投資は後発事業者にとっては大きな参入障壁になると考えております。また当社の開発品であるBNCT用ホウ素薬剤「SPM-011」は、厚生労働省の実施する先駆け審査指定制度※5の対象品目に指定されておりましたが、2020年3月にステボロニン®として医薬品製造販売承認を取得したことは後発事業者にとっては、先駆け審査指定制度の対象品目に指定されるための要件の一つとして治療薬の画期性が求められることから、参入障壁となると考えられ、当社の競争優位性は一定程度維持できると認識しております。
この競争優位性を維持しながら、ステボロニン®を「世界初、日本初」の医薬品として、医療現場へ提供することを目標として事業を推進してまいります。
[ステボロニン®の製造フロー]
(3)開発パイプライン
当社は、BNCT用ホウ素薬剤の適応疾患の拡大を開発テーマとして、適応疾患別に開発パイプラインを構成しております。開発パイプライン並びにそのスケジュール及び本書提出日までの進捗は次のとおりです。
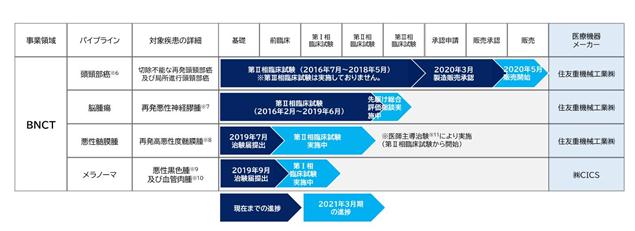
国内における開発パイプラインは、頭頸部癌及び再発悪性神経膠腫を対象に、住友重機械工業株式会社と共同で第Ⅱ相臨床試験を実施してまいりました。上記2疾患を先行してパイプラインとした理由は、外科的手術が困難な場合があること、再発悪性神経膠腫においては再発リスク・悪性度が高いこと、またBNCTの特徴として正常組織への影響が少ないことが主な理由であり、特に重要な器官が集中する脳及び頭頸部における疾患を選定しております。
頭頸部癌の第Ⅱ相臨床試験における主要評価項目は、BNCT施術後90日における奏効率(腫瘍縮小効果)とし、安全性に問題のある事象はなく、有効性は期待値を達成いたしました。その試験結果に基づき、医薬品製造販売承認申請を行い、2020年3月に、切除不能な局所進行又は局所再発の頭頸部癌を効能・効果として、製造販売承認を取得し、同年5月にはステボロニン®の販売を開始しております。
また、再発悪性神経膠腫の第Ⅱ相臨床試験における主要評価項目は、BNCT施術後1年における生存割合とし、安全性及び有効性についての評価を行い、現在は目標症例数全例のBNCT施術を完了しております。第Ⅱ相臨床試験の結果は、再発膠芽腫※724例の1年生存率が79.2%となり、試験開始前の設定期待値60%を超える結果となりました。当該試験結果をもって、先駆け審査指定制度の枠組みにおいて独立行政法人医薬品医療機器総合機構(以下「PMDA」という。)と一部変更申請に向けた協議を行っておりますが、当該試験の主要評価項目である生存率は、年齢やがんの組織型(grade)、術前術後の全身状態などの患者背景因子が予後に影響することから、患者背景因子の違いを排除した上で有効性を示す試験データが追加的に必要となる可能性があると判断しております。本書提出日現在では、PMDAとの協議を継続しておりますが、追加の臨床試験の実施が必要となった場合に備え、並行して試験計画の立案を進めております。
新たなパイプラインとしては、脳腫瘍の一種である再発高悪性度髄膜腫を対象に、大阪医科大学附属病院において医師主導治験により第Ⅱ相臨床試験が実施されております。当社は、本試験で使用される治験薬の提供を行っております。
さらに、皮膚がんの一種である悪性黒色腫及び血管肉腫を対象に、国立研究開発法人国立がん研究センターにおいて第Ⅰ相臨床試験を開始いたしました。本試験に使用される熱中性子の発生装置は株式会社CⅠCSが開発したものであり、同社との共同治験として実施しております。
国内における新規パイプラインは、治験実績及び臨床研究データを吟味した上で、BNCTの効果が高いと想定される疾患を慎重に選定し、ステボロニン®の更なる適応拡大を図ります。
(4)事業戦略
当社は、BNCTの医療技術を軸に加速器メーカーと共同でステボロニン®の適応拡大に向けた研究開発及び臨床試験を実施し、開発パイプラインの拡充を進めてまいります。またステボロニン®の医薬品製造販売承認を取得したことに伴い、国内ではBNCTによる医療技術や治療実績の認知度向上と加速器の普及を目指し事業を展開してまいります。 認知度の向上には医療施設や大学等の研究機関への訪問活動を通じてステボロニン®の有効性や安全性に係る医療情報の提供を充実させていくとともに、学会や講演会を通じて、より効果的な事業活動を展開してまいります。
海外では日本で承認を得た疾患を対象に、米国及び欧州を中心に承認取得を目指すとともに、各国のレギュレーションに通じた製薬企業等との連携によるアライアンスモデルを計画しており、パートナー企業の選定に取り組んでまいります。そして特に成長が見込まれる海外のオンコロジー領域におけるステボロニン®の適応拡大は当社における重要な成長戦略と位置づけ、経営資源の重点配分を行ってまいります。
当社は医薬品開発事業のみの単一セグメントであり、事業の系統図は下記のとおりです。
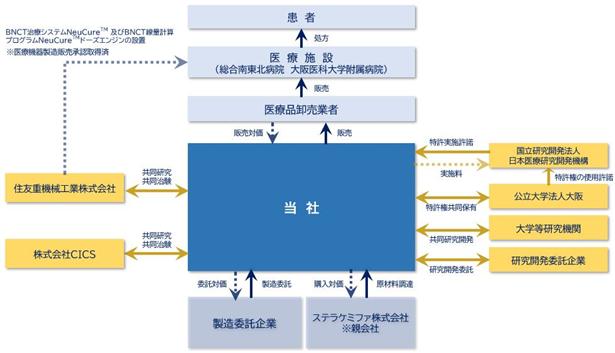
(5)開発戦略
当社では、研究開発拠点であるさかい創薬研究センターでステボロニン®の適応拡大等に向けた研究開発に取り組んでおります。またBNCTの拡張戦略として、18F-FBPA-PET※12に使用するPET薬剤の開発についても加速器メーカーと共同で取り組んでおります。
18F-FBPA-PETは、核医学検査の一つで、BNCTの有効成分であるボロファラン(10B)をPET核種である18Fで標識化することで、腫瘍の位置や範囲を画像として得ることができるだけでなく、ホウ素薬剤が腫瘍にどの程度取り込まれているか、BNCTの有効性をあらかじめ確認することが期待できます。
今後、BNCTの適応疾患の拡大を図る上で、18F-FBPA-PETの開発は重要な役割を担っております。
<語句説明>
※1「ボロファラン(10B)」
「4-ボロノ-L-フェニルアラニン(L-BPA)」と呼ばれるホウ素化合物であり、分子内にホウ素原子を一つ持っています。
※2「フェニルアラニン」
タンパク質を構成するアミノ酸で、食品中のタンパク質に多く含まれている必須アミノ酸の一つです。
※3「チロシン」
タンパク質を構成するアミノ酸で、動物の体内ではフェニルアラニンから合成されます。
※4「LAT-1」
L-type amino acid transporter-1(L型アミノ酸トランスポーター1)の略称。
細胞の増殖等に必要なアミノ酸の輸送に関わるタンパク質をアミノ酸トランスポーターと呼びます。アミノ酸トランスポーターは正常細胞にも存在しますが、LAT-1は多くのがん細胞に選択的かつ高発現するアミノ酸トランスポーターであり、フェニルアラニンやチロシンを輸送します。
※5「先駆け審査指定制度」
一定の要件を満たす新薬等について、厚生労働省が、開発の比較的早期の段階から薬事承認に係る相談・審査等において優先的な取扱いを行う制度です。具体的には、「①治療薬の画期性、②対象疾患の重篤性、③対象疾患にかかる極めて高い有効性、④世界に先駆けて日本で早期開発・申請する意思」の4つの要件を満たす画期的な新薬等を開発段階で対象品目に指定し、新たに整備された相談の枠組みを優先的に適用し、かつ優先審査を適用することにより、審査期間を6ヶ月(通常は12ヶ月)まで短縮することを目指すものとされています。なお、先駆け審査指定制度においては、対象品目の指定時に予定される効能又は効果も指定されることから、製造販売承認取得後に適応疾患を拡大する際には同制度の対象外となります。当社は、再発悪性神経膠腫と切除不能な局所再発頭頸部癌並びに局所進行頭頸部癌(非扁平上皮癌)について、対象品目の指定を受けておりましたが、2020年3月に、切除不能な局所再発頭頸部癌及び局所進行頭頸部癌を対象として、製造販売承認を取得しております。
※6「頭頸部癌」
頭頸部とは、脳の下側の顔面から鎖骨までの部分を示します。頭頸部癌とは、この範囲に含まれる、鼻、口、のど、上あご、下あご、耳などにできるがんのことです。頭頸部癌は、すべてのがんの約5%程度と考えられており、がんが発生する部位の種類が多く、発生原因、治療法、予後が異なることが特徴とされています。頭頸部には人間が生きる上で必要な器官が集中しており、その機能を温存できる治療法の確立が求められています。
※7「悪性神経膠腫」
神経膠腫とは、脳に発生する悪性腫瘍で原発性脳腫瘍の約30%を占めます。神経膠腫は、その悪性度によって4段階(グレードⅠ~Ⅳ)に分類され、中でもグレードⅢ~Ⅳに分類される悪性度が高い神経膠腫を悪性神経膠腫と呼び、さらにグレードⅣの神経膠腫を膠芽腫と呼びます。膠芽腫を含む悪性神経膠腫は、現在なお治療が困難な疾患とされています。
※8「高悪性度髄膜腫」
髄膜とは、脳と脊髄を保護している薄い組織層で、髄膜腫とはその内側の層の一つにできるがんのことです。髄膜腫は良性であることが多く、高悪性度髄膜腫は希少疾患である一方で、再発や転移を起こしやすい、治りにくい腫瘍の一つです。
※9「悪性黒色腫」
悪性黒色腫は皮膚がんの一つで、単に黒色腫又はメラノーマと呼ばれることもあります。皮膚の色と関係するメラニン色素を産生する皮膚の細胞で、表皮の基底層に分布しているメラノサイト又は母斑細胞が悪性化した腫瘍と考えられています。
※10「血管肉腫」
血管肉腫とは、血管の内皮細胞から発生するがんのことです。体のいたるところにできる可能性があり、皮膚に生じることが多いがんです。
※11「医師主導治験」
医師主導治験とは、製薬企業等と同様に医師自ら治験を企画・立案し、治験計画届を提出して実施する治験を指します。大阪医科大学附属病院において実施している再発高悪性度髄膜腫の臨床試験に使用されるホウ素薬剤は、当社から提供しています。
※12「18F-FBPA-PET」
がんの画面診断技術であるPET診断において、現在使用されている18F-FDGに代わる新たなPET薬剤として18F-FBPAの開発を行っています。18F-FBPAはBNCTの施術において、ステボロニン®の分布状況を可視化し、治療前にBNCTの効果を予測することも可能と考えられており、BNCTの発展に貢献するものと期待されています。
4【関係会社の状況】
|
名称 |
住所 |
資本金 (千円) |
主要な事業の内容 |
議決権の所有割合又は被所有割合 (%) |
関係内容 |
|
(親会社) ステラケミファ株式会社 (注1) |
大阪市中央区 |
4,829,782 |
高純度薬品事業 |
被所有 63.9 (注2) |
当社医薬品の原材料を製造 当社債務の保証 |
(注)1.有価証券報告書を提出しております。
2.本書提出日現在においては、被所有割合は63.4%となっております。
5【従業員の状況】
(1)提出会社の状況
|
|
|
|
|
2021年2月28日 |
|
従業員数(人) |
平均年齢(歳) |
平均勤続年数(年) |
平均年間給与(円) |
|
|
|
( |
|
|
|
|
事業部門の名称 |
従業員数(人) |
|
|
創薬研究部 |
10 |
(-) |
|
臨床開発部 |
4 |
(-) |
|
その他 |
22 |
(3) |
|
全社(共通) |
7 |
(-) |
|
合計 |
|
( |
(注)1.従業員数は就業人員であり、臨時雇用者数は、最近1年間の平均人員を( )外数で記載しております。
2.平均年間給与は、賞与及び基準外賃金を含んでおります。
3.当社は単一セグメントであるため、事業部門別の従業員数を記載しております。
4.全社(共通)として記載されている従業員数は、総務及び経理等の管理部門の従業員数であります。
(2)労働組合の状況
当社の従業員は、会社設立と同時に親会社であるステラケミファ株式会社が結成した労働組合であるステラケミファユニオンに加入しております。2021年2月28日現在の組合員数は22人であり、所属上部団体は日本労働組合総連合会です。なお、労使関係については、円滑な関係にあり、特記すべき事項はありません。