第二部【企業情報】
第1【企業の概況】
1【主要な経営指標等の推移】
|
回次 |
第2期 |
第3期 |
第4期 |
第5期 |
第6期 |
|
|
決算年月 |
2014年12月 |
2015年12月 |
2016年12月 |
2017年12月 |
2018年12月 |
|
|
事業収益 |
(千円) |
|
|
|
|
|
|
経常利益又は経常損失(△) |
(千円) |
|
|
|
△ |
△ |
|
当期純利益又は当期純損失(△) |
(千円) |
|
|
|
△ |
△ |
|
持分法を適用した場合の投資利益 |
(千円) |
|
|
|
|
|
|
資本金 |
(千円) |
|
|
|
|
|
|
発行済株式総数 |
(株) |
|
|
|
|
|
|
純資産額 |
(千円) |
|
|
|
|
|
|
総資産額 |
(千円) |
|
|
|
|
|
|
1株当たり純資産額 |
(円) |
|
|
|
|
|
|
1株当たり配当額 |
(円) |
|
|
|
|
|
|
(うち1株当たり中間配当額) |
( |
( |
( |
( |
( |
|
|
1株当たり当期純利益金額又は 1株当たり当期純損失金額(△) |
(円) |
|
|
|
△ |
△ |
|
潜在株式調整後1株当たり当期純利益金額 |
(円) |
|
|
|
|
|
|
自己資本比率 |
(%) |
|
|
|
|
|
|
自己資本利益率 |
(%) |
|
|
|
|
|
|
株価収益率 |
(倍) |
|
|
|
|
|
|
配当性向 |
(%) |
|
|
|
|
|
|
営業活動によるキャッシュ・フロー |
(千円) |
|
|
|
△ |
△ |
|
投資活動によるキャッシュ・フロー |
(千円) |
|
|
|
|
△ |
|
財務活動によるキャッシュ・フロー |
(千円) |
|
|
|
|
|
|
現金及び現金同等物の期末残高 |
(千円) |
|
|
|
|
|
|
従業員数 |
(人) |
|
|
|
|
|
|
(外、平均臨時雇用者数) |
( |
( |
( |
( |
( |
|
(注)1.当社は連結財務諸表を作成しておりませんので、連結会計年度に係る主要な経営指標等の推移については記載しておりません。
2.事業収益には、消費税等は含まれておりません。
3.持分法を適用した場合の投資利益については、当社は関連会社を有していないため記載しておりません。
4.1株当たり配当額及び配当性向については、配当を実施していないため記載しておりません。
5.潜在株式調整後1株当たり当期純利益金額については、第2期、第3期及び第4期は新株予約権が存在するものの、当社株式は非上場であるため、期中平均株価が把握できませんので記載しておりません。また、第5期及び第6期については、新株予約権が存在するものの、当社株式は非上場であるため、期中平均株価が把握できませんので、また、1株当たり当期純損失金額であるため記載しておりません。
6.第5期及び第6期の自己資本利益率については、当期純損失であるため、記載しておりません。
7.株価収益率については、当社株式は非上場であるため、記載しておりません。
8.第2期、第3期及び第4期については、キャッシュ・フロー計算書を作成していないため、営業活動によるキャッシュ・フロー、投資活動によるキャッシュ・フロー、財務活動によるキャッシュ・フロー並びに現金及び現金同等物の期末残高は記載しておりません。
9.第5期及び第6期の財務諸表については、「財務諸表等の用語、様式及び作成方法に関する規則」(1963年大蔵省令第59号)に基づき作成しており、金融商品取引法第193条の2第1項の規定に基づき、EY新日本有限責任監査法人の監査を受けております。
第2期、第3期及び第4期の財務諸表については、「会社計算規則」(2006年法務省令第13号)の規定に基づき算出した各数値を記載しております。また、当該各数値については、金融商品取引法第193条の2第1項の規定に基づくEY新日本有限責任監査法人の監査を受けておりません。
10.当社は、2016年12月8日開催の取締役会決議により、2017年1月13日付で普通株式1株につき5,000株の割合で株式分割を行っております。第5期の期首に当該株式分割が行われたと仮定し、1株当たり純資産額及び1株当たり当期純利益金額又は1株当たり当期純損失金額(△)を算定しております。
11.当社は、2017年1月13日付で普通株式1株につき5,000株の株式分割を行っております。
そこで、東京証券取引所自主規制法人(現 日本取引所自主規制法人)の引受担当者宛通知「『新規上場申請のための有価証券報告書(Ⅰの部)』の作成上の留意点について」(2012年8月21日付東証上審第133号)に基づき、第2期の期首に当該株式分割が行われたと仮定して算定した場合の1株当たり指標の推移を参考までに掲げると、以下のとおりとなります。
なお、第2期、第3期及び第4期の数値(1株当たり配当額についてはすべての数値)については、EY新日本有限責任監査法人の監査を受けておりません。
|
|
第2期 |
第3期 |
第4期 |
第5期 |
第6期 |
|
|
2014年12月 |
2015年12月 |
2016年12月 |
2017年12月 |
2018年12月 |
||
|
1株当たり純資産額 |
(円) |
0.25 |
54.01 |
82.38 |
64.12 |
100.39 |
|
1株当たり当期純利益金額又は1株当たり当期純損失金額(△) |
(円) |
0.14 |
1.45 |
9.21 |
△18.26 |
△1.06 |
|
潜在株式調整後1株当たり当期純利益金額 |
(円) |
― |
― |
― |
― |
― |
|
1株当たり配当額 (うち1株当たり中間配当額) |
(円) |
― (―) |
― (―) |
― (―) |
― (―) |
― (―) |
2【沿革】
当社は、大阪大学大学院医学系研究科の研究成果である機能性ペプチドを医薬品、化粧品及び医療機器等として開発することを目的として、2013年10月に設立した創薬系バイオベンチャーであります。
|
年月 |
事項 |
|
2013年10月 |
東京都渋谷区において株式会社ファンペップ(資本金1百万円)を設立 |
|
2015年3月 |
アンジェスMG株式会社(現アンジェス株式会社)との間で機能性ペプチド(SR-0379及びキュアペプチン等)の知的財産権の移転を伴う現物出資契約を締結 |
|
2015年4月 |
東京都港区に東京オフィスを新設 |
|
2015年6月 |
大阪府茨木市に大阪オフィスを新設 |
|
2015年7月 |
大阪大学との間で抗体誘導ペプチドに関する共同研究を開始 |
|
2015年10月 |
塩野義製薬株式会社との間で機能性ペプチドSR-0379に関するライセンス契約を締結 |
|
2016年1月 |
本店登記地を大阪府茨木市(大阪オフィス)に変更 東京都渋谷区に東京オフィスを移転 |
|
2016年2月 |
株式会社メディパルホールディングスとの間で抗体誘導ペプチドの研究開発に関する提携基本契約を締結 |
|
2016年9月 |
大日本住友製薬株式会社との間で標的タンパク質IL-17Aに関する抗体誘導ペプチドの共同研究を開始 |
|
2018年3月 |
大日本住友製薬株式会社との間で抗体誘導ペプチドFPP003に関するオプション契約を締結 |
|
2018年7月 |
塩野義製薬株式会社が機能性ペプチドSR-0379の皮膚潰瘍を対象とする日本での第Ⅱ相臨床試験を開始 |
|
2019年4月 |
抗体誘導ペプチドFPP003の尋常性乾癬を対象とするオーストラリアでの第Ⅰ/Ⅱa相臨床試験を開始 |
|
2019年5月 |
大阪府吹田市に千里オフィスを開設 大阪オフィスを彩都オフィスに改称 |
3【事業の内容】
当社は、医薬品等の研究開発事業の単一セグメントであるため、セグメントごとの情報は記載しておりません。
なお、「(*)」を付している用語及び出所については、「3 事業の内容」の末尾に用語解説及び参考文献を設け、説明しております。
当社は、大阪大学大学院医学系研究科の研究成果である機能性ペプチドの研究開発を進め、医薬品、化粧品及び医療機器等の事業分野に実用化することを主な事業としております。事業内容の詳細は以下のとおりであります。
(1)ビジネスモデル
① 機能性ペプチドについて
当社は、自らの技術領域を、機能性ペプチドを基礎とする領域及びこれとシナジーを有する関連する領域としております。
(A)生命維持の仕組み
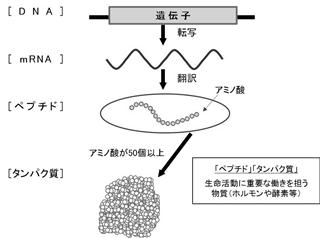
ヒトの体は約60兆個の細胞で構成されており、それぞれの細胞には約30億個の塩基配列からなるDNAが存在し、このDNAに2万~3万種類の遺伝子が含まれております。遺伝子にスイッチが入ると、その塩基配列情報がmRNAとしてコピー(「転写」といいます)され、更にmRNAの塩基配列情報に基づき、体内のアミノ酸(体内には20種類あります)が結合していき、アミノ酸配列が形成(「翻訳」といいます)され、生理活性(機能性)を持ったタンパク質が産生されます。ヒトの生命活動は、約60兆個の細胞において、それぞれの細胞内で約2~3万種類の遺伝子がとてもバランス良く働き、最終的にはタンパク質という形で機能を発揮することで維持されております。
<遺伝子からタンパク質が産生される仕組み>
|
|
(B)「機能性ペプチド」とは?
ペプチドとは、アミノ酸が2~50個程度が結合した物質であります。一般的に、50個以下のアミノ酸が鎖状に結合した物質をペプチドと呼び、それ以上の数のアミノ酸が結合した物質をタンパク質と呼んでおります。
ペプチドの中には、生体内等で機能を発揮するものがあり、「機能性ペプチド」と呼ばれています。機能性ペプチドは、医薬品、化粧品及び食品等の幅広い事業分野で実用化されています。
例えば、生体内のペプチドには、体内の器官の働きを調整するための情報伝達を担うホルモン等(インスリン(*)、グルカゴン、カルシトニン等が含まれます)があり、タンパク質のように生体内で機能を担っております。これらのホルモン由来の機能性ペプチドは、がんや糖尿病領域の医薬品として発売されております。また、タンパク質の分解過程で生じるペプチドが機能を持っていることもあり、血圧降下ペプチド等の特定保健用食品等の食品分野や、スキンケアやヘアケア商品として化粧品分野で利用されています。
<機能性ペプチドを利用した主な医薬品及び食品>
|
分野 |
領域 |
機能性ペプチド |
売上高 |
|
医薬品 |
糖尿病 |
インスリン製剤(ホルモン関連) |
2兆3,615億円(注)1 |
|
|
がん他 |
リュープロレリン(ホルモン関連) |
1,101億円(注)2 |
|
|
|
ゴセレリン(ホルモン関連) |
752百万ドル(注)3 |
|
|
免疫抑制 |
シクロスポリン |
488百万ドル(注)4 |
|
食品 |
血圧降下 |
イワシペプチド、ラクトトリペプチド、 |
― |
(注)1.出所:TPCマーケティングリサーチ株式会社「2018年 世界のバイオ医薬品市場」
2.出所:武田薬品工業株式会社「IR資料」
3.出所:AstraZeneca社「IR資料」
4.出所:Novartis社「IR資料」
② 当社の特徴について
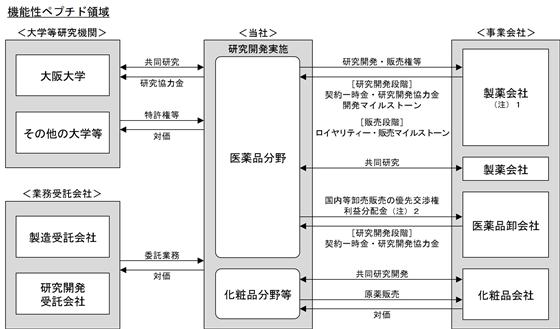
当社の事業系統図は、以下のとおりであります。
<当社の事業系統図>
|
|
(注)1.研究開発・販売権等のライセンス契約を締結する前に、その契約締結に対するオプションを付与するオプション契約を締結する場合もあります。
2.株式会社メディパルホールディングスとの提携契約に基づき、抗体誘導ペプチドプロジェクトから創出した医薬品を製薬会社に導出した際には、当社は同社に対し「利益分配金」として、製薬会社から受け取る契約一時金及び開発マイルストーンの一部を支払う予定であります。
当社は機能性ペプチドを幅広い分野において応用していく方針でありますが、ビジネスモデルの特徴については、現時点での事業計画に対して影響が大きい医薬品分野での事業展開を中心に記載しております。
(A)大学発ベンチャーの役割
当社は、大阪大学発の創薬系バイオベンチャー企業であり、大学の研究成果を製薬会社への橋渡しに向けてインキュベート(研究開発を推進)する役割を担っております。この役割を担うため、当社は、大阪大学を始めとする大学等の研究機関との間で、共同研究等により連携を図り、大学の技術シーズを生かした基礎研究を実施しております。更に、当社は、医薬品の研究開発プロセスのうち、基礎研究から、臨床試験で初期の有効性や安全性を確認する早期探索的臨床試験(一般的には、第Ⅱ相臨床試験)までを自社で実施可能な範囲とし、技術シーズのインキュベーションを行う方針であります。
<一般的な医薬品の研究開発プロセスの内容>
|
プロセス |
期間 |
主な内容 |
|
|
基礎研究 |
2~3年 |
新薬候補化合物の探索(合成及び絞込み等)研究 |
|
|
前臨床試験 |
3~5年 |
実験動物等を用いて有効性及び安全性等を確認する試験 |
|
|
臨床試験 |
3~7年 |
第Ⅰ相 |
少数の健康な人を対象に安全性等を確認する試験 |
|
第Ⅱ相 |
少数の患者を対象に有効性及び安全性を探索的に確認する試験 |
||
|
第Ⅲ相 |
多数の患者を対象に有効性と安全性を検証的に確認する試験 |
||
|
申請・承認 |
1~2年 |
各国の規制当局による審査 |
|
(注)臨床試験開始前に実施する非臨床試験を前臨床試験といいます。
(B)製薬会社との提携体制
医薬品の研究開発は期間が長く必要資金も大きいのが特徴であります。当社が実施する可能性がある早期探索的臨床試験まででさえ、少なくとも数年間にわたる年月と数億円の資金が必要であります。このため、当社は、研究開発の早期段階から製薬会社等との提携体制を構築し、その提携収入等により、研究開発遂行上の財務リスクの低減を図っていく方針であります。
一般的な提携形態としては、基礎研究段階では共同研究契約等、前臨床試験や臨床試験段階ではライセンス契約を締結して、製薬会社と当社の間で研究開発段階や商業化段階の役割分担と経済条件を決めます。また、ライセンス契約に先行して、その契約締結に対するオプションを供与するオプション契約を締結する場合もあります。当社の場合は、機能性ペプチドSR-0379は塩野義製薬株式会社との間でライセンス契約、抗体誘導ペプチドFPP003は大日本住友製薬株式会社との間でオプション契約を締結しており、抗体誘導ペプチドの研究開発に関しては、株式会社メディパルホールディングスとの間で研究開発支援契約、大日本住友製薬株式会社との間で精神神経領域の抗体誘導ペプチドの研究契約、塩野義製薬株式会社との間で疼痛領域の抗体誘導ペプチドの共同研究契約を締結しております。また、抗ウイルス剤の研究については、富士フイルム株式会社と共同研究を実施しております(それぞれの提携契約の内容は、「(2)研究開発パイプライン」をご参照ください)。
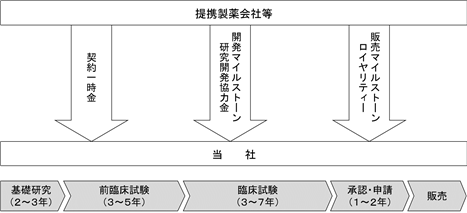
これらの提携体制のもと、当社の主な事業収益は、提携製薬会社等からの収入であり、医薬品の研究開発段階においては、契約一時金、研究開発協力金及び開発マイルストーン、販売段階においては、ロイヤリティー及び販売マイルストーンを想定しております。当社は、現時点で事業収益に計上しているのは研究開発段階の収入のみであり、これらの収入により研究開発投資による財務リスク低減を図りながら研究開発を進めております。そして、当社開発品が将来上市に至った場合に提携製薬会社から受け取るロイヤリティー収入によって本格的な利益拡大を実現する計画であります。
<医薬品の開発プロセスと提携会社から受け取る一般的な収益>
|
|
<主な収益の内容>
|
収入名 |
内容 |
|
契約一時金 |
契約締結時に一時金として受け取る収益 |
|
開発マイルストーン |
研究開発の進捗に応じて、事前に設定したイベントを達成した際に受け取る収益 |
|
研究開発協力金 |
研究開発を推進するために提携会社から受け取る収益 |
|
ロイヤリティー |
医薬品販売後に、年間販売額に応じて受け取る収益 |
|
販売マイルストーン |
医薬品販売後に、事前に設定した年間販売額を達成した際に受け取る収益 |
(C)業務受託会社の活用
当社は、研究開発に従事する中で、当社が研究開発戦略を描いたうえで、製造及び研究開発に関する業務を積極的に外部委託しております。これにより、当社は、製造施設や試験施設を保有することなく、少人数制による低い固定費で研究開発を推進することができ、財務リスクの低減を図っております。
(2)研究開発パイプライン
当社の研究開発パイプラインは、機能性ペプチドの研究テーマ及び開発品により構成されております。
研究開発パイプラインは、「AG-30由来の機能性ペプチド」、「抗体誘導ペプチド」及び「抗ウイルス剤」の主に3種類に分類されます。
<医薬品>
・ 開発品
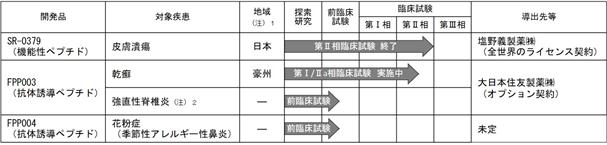
(注)1.地域は、臨床試験の実施地域のことであります。
2.国立研究開発法人日本医療研究開発機構(AMED)「創薬支援推進事業・希少疾病用医薬品指定前実用化支援事業」の支援を受けて実施しています。
・ 研究テーマ
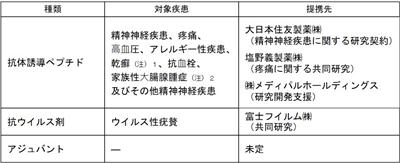
(注)1.乾癬に関する抗体誘導ペプチドの研究については、FPP003(IL-17A)とは異なる標的タンパク質(IL-23)を対象にしております。
国立研究開発法人新エネルギー・産業技術総合開発機構(NEDO)「研究開発型ベンチャー支援事業/橋渡し研究開発促進による事業化支援」の支援を受けて、橋渡し研究機関大阪大学との共同研究により実施しています。
2.国立研究開発法人日本医療研究開発機構(AMED)「医療分野研究成果展開事業・産学連携医療イノベーション創出プログラム セットアップスキーム(ACT-MS)」の支援を受けて、香川大学、大阪大学及び京都府立医科大学との産学連携により実施しています。
<化粧品等>
当社は、株式会社ファンケルとの間で共同研究開発を行った結果、当社の機能性ペプチドを含有するシャンプーとして、2018年3月に「マイルドクレンジングシャンプー」、同年6月に「ボリュームアップシャンプー」が発売されました。
これらの商品販売により、当社は、化粧品原料商社を通してペプチド原薬販売収入を受領しております。
① AG-30由来の機能性ペプチド
AG-30(angiogenic peptide-30)は、大阪大学大学院医学系研究科において、新規血管新生因子の探索研究の中で同定された機能性ペプチド(30アミノ酸)で、血管新生作用を持っております。更に、抗菌活性を併せ持つ創薬シーズであります。
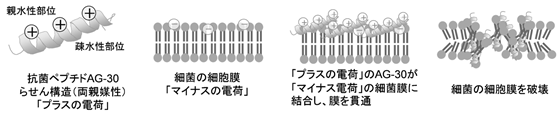
ヒト生体内には「抗菌ペプチド」と呼ばれる20~40個のアミノ酸から構成される一群のペプチドが皮膚や免疫細胞に存在し、免疫防御機能の一翼を担っております。「抗菌ペプチド」は、プラスに荷電している親水性(*)のアミノ酸と疎水性(*)のアミノ酸が偏在するという構造的特徴により、細菌や真菌の細胞膜を破壊して抗菌作用を示します。AG-30は、天然に存在する「抗菌ペプチド」と類似の構造的特徴を持つことから、同様の作用メカニズムで抗菌活性を示すと考えられます。
<抗菌ペプチドの抗菌作用メカニズム>
|
|
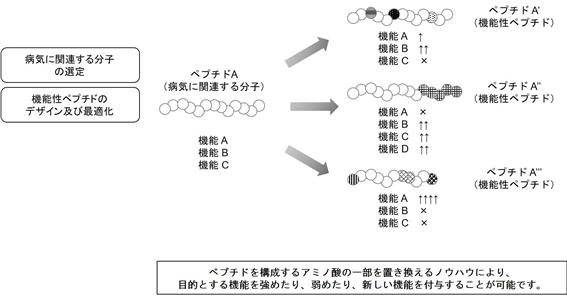
当社の研究者は、AG-30を起源とし、そのペプチドを構成するアミノ酸の一部を置き換える検討を重ねることで、目的とする機能が増強したペプチド、新しい機能が付与されたペプチド又は多機能の活性を示すペプチドの特定の機能が消失しているペプチドを見出し、SR-0379、AJペプチド及びキュアペプチンを同定してまいりました。
■ プラットフォーム技術「SPIRIT(Smart PeptIde Research Integrated Technology)」
当社は、AG-30を改変してSR-0379、AJペプチド及びキュアペプチン等を創製してきた当社研究員の経験に基づき、目的とする機能を持った機能性ペプチドを創製する技術ノウハウを保有しております。更に、機能性ペプチド特有の投与方法や品質管理に関する技術ノウハウも保有しております。
これらの技術ノウハウは、抗菌ペプチドの一種であるAG-30に限らず、ホルモン等の他の病気に関連する分子を起源とする機能性ペプチドの創製にも応用が可能なものであり、新規の機能性ペプチドを創製するにあたっての当社のプラットフォーム技術に位置付けております。
なお、当社は、これらの技術ノウハウのことを「SPIRIT」と呼んでおります。
<プラットフォーム技術「SPIRIT」の主な内容>
|
|
(A)SR-0379
◇ 概要
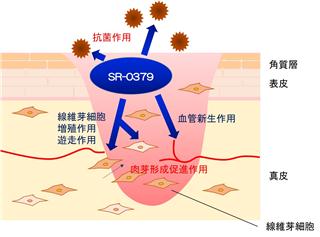
SR-0379は、AG-30を起源とし、生体内安定性や製造コストを改良し、医薬品として最適化を図った開発化合物であります。また、SR-0379は、血管新生や肉芽(*)形成促進を主たる作用とし、抗菌活性を併せ持った機能性ペプチドで20個のアミノ酸からなります。
<SR-0379の作用メカニズム>
|
|
◇ 対象疾患
SR-0379の対象疾患は、難治性皮膚潰瘍であります。皮膚潰瘍は、皮膚の組織が一定程度、表皮を超えて欠損した状態であります。外傷や手術創等の急性皮膚潰瘍は一般的に正常な創傷治癒メカニズムが働くことで治癒することが期待できますが、創傷の局所環境や基礎疾患により創傷治癒メカニズムが十分に働かない場合には、難治性皮膚潰瘍となります。難治性皮膚潰瘍には、長期間、圧力がかかった箇所に生じる「褥瘡(じょくそう(いわゆる「床ずれ」))」、糖尿病を合併する「糖尿病性潰瘍」や主に静脈うっ血を原因とする「下腿潰瘍」等があります。
このような難治性皮膚潰瘍の治療は、創傷治癒メカニズムを促進することが重要であります。SR-0379は、「創傷治癒を遅延させる要因」である感染を防御及び予防する機能を備えた上で、「創傷治癒を促進する要因」の血管新生作用や肉芽形成促進作用等により創傷治癒メカニズムを促進します。
皮膚潰瘍の患部に消毒剤を用いる場合には、その組織障害性から創傷治癒を遅延させることが懸念されますが、SR-0379にはその懸念がなく、抗菌作用により健康な皮膚の持つ感染防御機能を補いながら、創傷治癒を促進させる新しいタイプの皮膚潰瘍治療剤として期待されます。
難治性皮膚潰瘍の患者数は多く、糖尿病性潰瘍患者は、糖尿病患者5,790万人(日本723万人、米国3,018万人、欧州主要5ヶ国2,048万人(出所:IDF「Diabetes Atlas 2017」)の5~10%程度(当社推定)が見込まれます。また、褥瘡患者数は米国で50万人(出所:Russo et al.(2008)(*))、下腿潰瘍患者数は米国で60万人(出所:Bowman et al.(1999)(*))との報告があります。
◇ 技術導入状況
当社は、2015年3月に、アンジェスMG株式会社(現アンジェス株式会社)との間で現物出資契約を締結し、同社よりSR-0379の知的財産権を取得しております。
◇ 開発状況
SR-0379の臨床試験は、日本において、2014年10月から健常人を対象とする第Ⅰ相臨床試験、2015年10月から難治性皮膚潰瘍患者(糖尿病性皮膚潰瘍、下腿潰瘍)を対象とする第Ⅰ/Ⅱa相臨床試験(試験①)、更に2017年9月からWerner症候群の皮膚潰瘍患者を対象とする第Ⅱ相臨床試験が医師主導治験として行われました(試験①は、大阪大学との契約に基づき、当社が資金面及び労務面での支援を実施いたしました)。更に、2018年7月からは、提携先の塩野義製薬株式会社が日本で皮膚潰瘍患者(褥瘡、糖尿病性皮膚潰瘍)を対象とする第Ⅱ相臨床試験(試験②)を実施いたしました。第Ⅰ/Ⅱa相臨床試験(試験①)及び第Ⅱ相臨床試験(試験②)の結果概要は下記のとおりであります。これらの試験結果等に基づき、本書提出日現在、次相臨床試験の準備が進んでおります。
[ 第Ⅰ/Ⅱa相臨床試験(医師主導治験)結果 ]
第Ⅰ/Ⅱa相臨床試験(プラセボ対照二重盲検ランダム化比較試験(*))においては、有効性に関しては、主要評価項目(*)とした最終評価時(投与4週目又は中止時)の潰瘍面積縮小率(%,平均値±標準偏差)は、プラセボ群(3例)で9.95±65.49、0.02%群(3例)で44.73±41.26、0.1%群(3例)で68.25±28.98、0.5%群(3例)で71.61±49.17でした。潰瘍面積の縮小率において、用量相関(*)的な増加傾向があり、高用量群でプラトーに達したと考察されました。また、安全性に関しては、治験薬と因果関係がある有害事象はありませんでした。4例に6件の有害事象が発現しましたが、1件はプラセボ群のものであり、6件いずれも因果関係が否定されました。(出所:UMIN臨床試験登録システム(*))
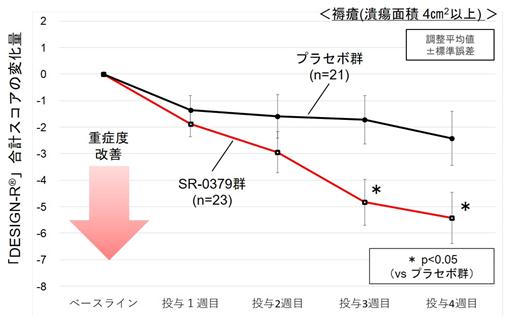
[ 第Ⅱ相臨床試験結果 ]
第Ⅱ相臨床試験(プラセボ対照二重盲検ランダム化比較試験)の有効性に関しては、重症度の高い褥瘡患者(潰瘍面積4㎠以上)のサブグループにおいて、0.1%群はプラセボ群に対し、実臨床で広く使用されている重症度に関する有効性評価指標「DESIGN-R®」合計スコア(*)を統計学的有意に改善しました(主要評価項目の「潰瘍面積の縮小率」では統計学的有意差に至りませんでした。)。また、安全性に関しては、治験薬と因果関係がある有害事象はありませんでした。
<有効性評価指標「DESIGN-R®」合計スコアの推移>
|
|
◇ 提携状況
当社は、2015年10月に、塩野義製薬株式会社との間でライセンス契約を締結し、SR-0379の全世界における独占的研究開発・商業化権を供与しております。なお、本提携では、当社は非臨床試験の一部(作用機序解析)を担当しております。
この契約により、当社は、契約時に一時金を受け取ったほか、SR-0379の研究開発の進捗に伴い、開発マイルストーンを受け取る予定であります。更に製品上市後には、販売額に応じたロイヤリティー及び販売マイルストーンを受け取る予定であります。
(B)AJペプチド
◇ 概要
アジュバント(*)は、感染症やがんなどのワクチンに含有される物質で、標的タンパク質(病気の原因となるタンパク質)に対する免疫反応を増強する役割を担っています。
AG-30を起源とし、アジュバント機能を増強したのが20個のアミノ酸からなるAJペプチドであります。当社は、AJペプチドを抗体誘導ペプチドのキャリア(*)として利用しております(詳細は、「② 抗体誘導ペプチド」のプラットフォーム技術「STEP UP(Search Technology of EPitope for Unique Peptide vaccine)」をご参照ください)。更に、今後も、AJペプチドの改良研究を実施していく方針であります。
◇ 技術導入状況
当社は、2016年11月に、アンチエイジングぺプタイド株式会社より、AJペプチドの医薬品分野の独占的な実施権の許諾を受けております。
(C)キュアペプチン
◇ 概要
AG-30を起源とし、血管新生作用を持たず、幅広い抗菌活性を持つ機能性ペプチドとして最適化を図ったのが20個のアミノ酸からなるキュアペプチンであります。
キュアペプチンは、AG-30及びSR-0379と同様に、その構造的特徴から、細菌や真菌の細胞膜を破壊することによって抗菌作用を示します。
◇ 技術導入状況
当社は、2015年3月に、アンジェスMG株式会社(現アンジェス株式会社)との間で現物出資契約を締結し、同社よりキュアペプチンの知的財産権を取得しております。
キュアペプチン含有商品については、その抗菌活性を生かした化粧品及び医療機器分野への応用を検討しております。
② 抗体誘導ペプチド
抗体誘導ペプチドは、標的タンパク質の働きを阻害する抗体(*)(ヒト免疫システム(*)の「獲得免疫(*)」の一種で「液性免疫」(*)と呼ばれます)を体内で産生させる機能性ペプチドであります。当社は、免疫システムに標的タンパク質の情報を記憶させることで、数ヶ月に一回の投与で抗体を維持し、薬効を持続させる長期作用型医薬品として、抗体誘導ペプチドの研究開発を進めております。
獲得免疫システムを医療へ応用した事例としては、外来病原体(インフルエンザ、BCGやポリオ等)に対する感染症予防ワクチンが広く普及しております。感染症予防ワクチンも、獲得免疫システムに病原体の情報を記憶させることで、ワクチンの種類によっては、数ヶ月間から数年間、場合によっては生涯にわたって予防効果を期待できる医薬品であります。
同じ獲得免疫システムを利用したものでありますが、感染症予防ワクチンと抗体誘導ペプチドの主要な違いの一つは、感染症予防ワクチンが外来病原体を標的とするのに対し、抗体誘導ペプチドは患者体内の自己タンパク質を標的としていることであります。このため、抗体誘導ペプチドは、(正常な自己細胞を攻撃して)副作用の原因となる細胞傷害性T細胞(*)(「獲得免疫」の一種で「細胞性免疫(*)」と呼ばれます)を活性化させず、薬の効果をもたらす抗体産生に関連するB細胞(液性免疫)のみを選択的に活性化させる技術的な工夫がなされております。
獲得免疫のうち「液性免疫」(抗体産生)のみを選択的に活性化させることから、当社は、この機能性ペプチドを「抗体誘導ペプチド」と呼んでおります。
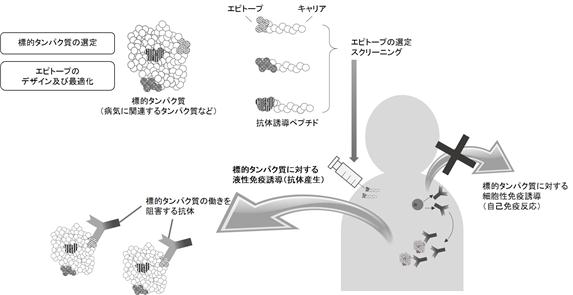
■ プラットフォーム技術「STEP UP(Search Technology of EPitope for Unique Peptide vaccine)」
当社は、大阪大学との共同研究等により、抗体誘導ペプチドのエピトープ(*)を選定する技術ノウハウを保有しております。このエピトープは、標的タンパク質に対する液性免疫は誘導するものの、細胞性免疫は誘導しないように設計する必要があります。
また、抗体誘導ペプチドは免疫システムを利用したワクチンの一種であり、免疫応答を誘発させるキャリアや、免疫反応を増強する物質であるアジュバントが必要になります。当社は、AG-30由来のAJペプチドを、アジュバント機能を併せ持ったキャリアとして期待し、抗体誘導ペプチドに利用しております。AJペプチドの利用により、キャリアに対する抗体(薬剤に対する抗体)産生による効果減弱等が発生しないなど、既存ワクチンに利用されているキャリアによる様々な問題を解決できる可能性があり、当社独自の強みと考えております。
これらのプラットフォーム技術は、病気に関連する様々な標的タンパク質に対する抗体誘導ペプチドの創製に応用が可能なものであり、当社は、今後も、これらのプラットフォーム技術にもとづき、新規の抗体誘導ペプチドを次々と創製していく方針であります。
なお、当社は、新規の抗体誘導ペプチドの創製に関するプラットフォーム技術を「STEP UP」と呼んでおります。
[ AI活用に関する共同研究 ]
当社は、2018年7月、フューチャー株式会社との間で、新規抗体誘導ペプチドの創製に関するプラットフォーム技術を強化する目的で、エピトープ選定及びキャリア改良研究を支援するAIシステム構築に関して共同研究契約を締結しております。
<プラットフォーム技術「STEP UP」の主な内容>
|
|
[ 抗体誘導ペプチドの特長 ]
・高価な抗体医薬の代替技術を目指す
抗体誘導ペプチドは、体内で抗体を長期間にわたって産生させる作用を持つことから、バイオ製造施設で人工的に製造する高価な抗体医薬に対して、安価な代替技術となることを目指しております(患者一人当たりの年間投与量は、抗体医薬が少なくともグラム(=1,000ミリグラム)レベルが必要であるのに対し、抗体誘導ペプチドはミリグラムレベルで可能と予想されます(出所:Bachmann et al.(2013)(*))。
抗体医薬は、全世界の市場規模が2017年度に前年度比20.3%増の11兆6,810億円(出所:TPCマーケティングリサーチ株式会社「2018年 世界のバイオ医薬品市場」)と市場が急拡大しておりますが、その一方で、薬剤費が高価で患者に対する経済的負担や医療財政上の問題が生じております。抗体医薬の安価な代替技術になり得る抗体誘導ペプチドは、高齢化社会を迎え増々関心が高まる医療財政上の問題解決に貢献する可能性を秘めております。
<抗体医薬と抗体誘導ペプチドの違い>
|
|
<抗体医薬の売上高上位15製品>
|
ブランド |
標的タンパク質 |
領域 |
2017年売上高 |
|
Humira |
TNF-α |
炎症 |
2兆1,373億円 |
|
MabThera/Rituxan |
CD20 |
がん・炎症 |
8,459億円 |
|
Herceptin |
HER2 |
がん |
7,996億円 |
|
Avastin |
VEGF |
がん |
7,624億円 |
|
Remicade |
TNF-α |
炎症 |
7,341億円 |
|
Opdivo |
PD-1 |
がん |
6,492億円 |
|
Stelara |
IL-12/23p40 |
炎症 |
4,533億円 |
|
Keytruda |
PD-1 |
がん |
4,304億円 |
|
Lucentis |
VEGF |
眼科 |
3,745億円 |
|
Soliris |
CD5 |
その他 |
3,553億円 |
|
Simponi |
TNF-α |
炎症 |
3,054億円 |
|
Xolair |
IgE |
呼吸器 |
3,026億円 |
|
Perjeta |
HER2 |
がん |
2,503億円 |
|
Prolia |
RANKL |
骨 |
2,501億円 |
|
Cosentyx |
IL-17A |
炎症 |
2,366億円 |
(出所:TPCマーケティングリサーチ株式会社「2018年 世界のバイオ医薬品市場」)
・生活習慣病等の「服薬コンプライアンス」の問題を解決へ
抗体誘導ペプチドは、獲得免疫システムを利用していることから、長期間にわたって標的タンパク質の働きを阻害できることが特徴であります。抗体誘導ペプチドは、既存医薬品と比較し、投与回数を数ヶ月に一度に改善することで、患者の利便性向上を図るとともに、特に生活習慣病治療薬で問題となっている服薬コンプライアンス上の問題(医師の指示どおりに、医薬品を服用しないという問題)を解決することが期待されます。生活習慣病治療薬は明確な症状がない場合が多く、また服薬管理を自ら行うことが難しい高齢者の患者が多いことから、服薬管理が良好な患者の割合は低い水準(米国において実施された高脂血症治療薬の服薬状況の調査では25~40%(出所:Jackevicius et al.(2002)(*))に留まっております。このため、抗体誘導ペプチドのような長期作用型医薬品が導入されれば、生活習慣病を適正にコントロールでき、心血管イベント等の合併症の発生を予防できる患者の割合が増えるものと考えられます。
以上の医療ニーズ及び社会ニーズを満たすために、生活習慣病のような慢性疾患に対する抗体誘導ペプチドは、当社のみならず世界各地で、アルツハイマー病、パーキンソン病、高血圧、高脂血症、がん、アレルギー性喘息及び糖尿病等を対象疾患として研究開発が行われております。
[ 研究開発支援に関する提携 ]
当社は、2016年2月に、株式会社メディパルホールディングスとの間で抗体誘導ペプチドの研究開発支援に関する提携契約を締結しております。
これにより、当社は、契約時に一時金を受け取ったほか、2016年4月以降の3年間にわたって研究開発協力金を受け取りました。一方、その対価として、株式会社メディパルホールディングスは、当社が抗体誘導ペプチドプロジェクトから創出したペプチド医薬品候補を製薬会社に導出した際には、当社が導出先から受け取る契約一時金及び開発マイルストーンの一部を受け取るほか、当該ペプチド医薬品の日本国内等の卸売販売について優先交渉権を取得する予定であります。
(A)FPP003
◇ 概要
FPP003は、IL-17A(Interleukin 17A)を標的タンパク質とする抗体誘導ペプチドであります。
IL-17Aは、免疫反応に関するサイトカイン(*)の一つであり、乾癬及び強直性脊椎炎に関与していることが明らかになっています。
◇ 対象疾患
FPP003の対象疾患は、尋常性乾癬及び強直性脊椎炎であります。
尋常性乾癬は乾癬の一種であり、皮膚の慢性炎症性疾患であります。尋常性乾癬の症状は、表皮細胞が異常に増殖し、境界明瞭な紅斑(皮膚が発赤する状態)が現れ、その表面に鱗屑(りんせつ、銀白色のうろこ状のかさぶた)が厚く付着してボロボロと剥がれ落ちるというものであり、患者様の生活の質(Quality of Life)の低下が問題となります。
乾癬の患者数は、米国では約750万人(出所:The American Academy of Dermatology(*))と多く、日本でも約43万人(出所:Kubota et al.(2015)(*))と推計されております。このうち、「軽症から中等症」の患者が約80%、皮疹範囲が体表面積の5%以上にも及ぶ「中等症から重症」の患者は約20%であります(出所:The American Academy of Dermatology)。乾癬患者全体のうち、上記の尋常性乾癬患者がほとんどで、約80~90%を占めております(出所:The American Academy of Dermatology)。
尋常性乾癬の治療は、「軽症から中等症」患者に対しては外用剤が使用され、「中等症から重症」患者に対しては光線療法や全身療法が行われておりますが、これらの治療法で効果が不十分な場合には、様々な標的タンパク質に対する抗体医薬が使用されております。IL-17Aに対する抗体医薬は2015年より日本及び米国で発売されております。
FPP003は、長期間に渡り治療効果が持続することが特徴であり、既存の抗体医薬と比較し、投与間隔が長く利便性の高い長期作用型医薬品として、市場に浸透することを目指しております。
一方、強直性脊椎炎は青年期に発症する脊椎と仙腸関節を主な病変部位とする原因不明の全身性の慢性炎症性疾患であります。病変部位では靭帯と骨との付着部位に炎症・骨化が起こり、疼痛、膨張、運動制限等がみられ、重症例では、脊椎の強直をきたして日常生活能力の著しい低下をもたらします。
強直性脊椎炎の治療には、非ステロイド性抗炎症剤(NSAIDs)が使用されておりますが、効果が不十分な場合や副作用の問題がある場合には、抗体医薬が使用されております。
日本において、希少疾病である強直性脊椎炎に対する研究開発は、国立研究開発法人日本医療研究開発機構(AMED)「創薬支援推進事業・希少疾病用医薬品指定前実用化支援事業」の支援を受けて実施しており、FPP003が将来の治療選択肢になることを目指しております。
◇ 技術導入状況
当社は、2018年8月に、大阪大学より、FPP003を含む抗体誘導ペプチドの独占的な実施権の許諾を受けております(対象の特許を受ける権利は、大阪大学と当社の共同所有)。
◇ 開発状況
FPP003は、大阪大学及び大日本住友製薬株式会社との共同研究のもとで当社が同定した開発化合物であります。
動物を用いた薬効試験では、乾癬モデルマウスに対する皮膚症状改善効果、脊椎関節炎モデルラットに対する関節炎症状の改善効果が示されています(強直性脊椎炎は、脊椎関節炎の一種であります)。
本書提出日現在、当社が尋常性乾癬を対象とするオーストラリアでの第Ⅰ/Ⅱa相臨床試験及び強直性脊椎炎を対象とする前臨床試験を実施中であります。
◇ 提携状況
当社は、2018年3月に、大日本住友製薬株式会社との間でオプション契約を締結いたしました。
このオプション契約により、大日本住友製薬株式会社は、当社が実施する初期臨床試験結果にもとづき、北米での全疾患に対する独占的開発・商業化権を取得する権利を保有しております。さらに北米以外の地域については、優先交渉権を保有しております。その対価として、当社は、契約時に一時金を受取ったほか、FPP003の研究開発の進捗に伴い、開発マイルストーンを受取る予定であります。
さらに、同社が上記のオプション権を行使した場合、当社は、一時金、FPP003の研究開発の進捗に伴い、開発マイルストーンを受取る予定であります。更に製品上市後には、販売額に応じたロイヤリティー及び販売マイルストーンを受取る予定であります。
(B)FPP004
◇ 概要
FPP004は、IgE(Immunoglobulin E)を標的タンパク質とする抗体誘導ペプチドであります。
IgEは、アレルギー反応に重要な役割を果たしており、アレルギー性疾患の発症に関与しております。
◇ 対象疾患
花粉症は、スギやヒノキの花粉により発症する季節性アレルギー性鼻炎であり、主な症状としては、発作性反復性のくしゃみ、(水様性)鼻漏及び鼻閉であります。
花粉症患者数については、厚生労働省の協力による全国調査により国民の約25%(出所:平成22年度厚生労働科学研究補助金 免疫アレルギー疾患予防・治療研究事業より(*))と考えられています。
IgEに対する抗体医薬は、アレルギー性疾患である気管支喘息及び慢性蕁麻疹を対象に2003年から世界各国で販売されてきましたが、花粉症に対しては、既存治療でコントロール不十分な重症又は最重症のスギ花粉症患者に対する有効性及び安全性を臨床試験で示し、2018年に日本で承認申請されております。
既存の抗体医薬は2週間又は4週間1回の投与が必要ですが、FPP004は長期間に渡り治療効果が持続することが特徴であり、既存の抗体医薬と比較し、投与間隔が長く利便性の高い長期作用型医薬品として市場に浸透することを目指しております。
◇ 開発状況
FPP004は、大阪大学との共同研究のもとで当社が同定した開発化合物であります。
本書提出日現在、前臨床試験を実施中であります。
(C)新規抗体誘導ペプチドの研究テーマ
当社は、大阪大学及びその他の大学との共同研究により、FPP003及びFPP004のほか、疼痛、高血圧、アレルギー性疾患、乾癬、抗血栓及び家族性大腸腺腫症(*)等の慢性疾患を対象に抗体誘導ペプチドの探索研究も進めております。
なお、家族性大腸腺腫症を対象とする抗体誘導ペプチドの研究については、国立研究開発法人日本医療研究開発機構(AMED)「医療分野研究成果展開事業・産学連携医療イノベーション創出プログラム セットアップスキーム(ACT-MS)」の支援を受けて、香川大学、大阪大学及び京都府立医科大学との産学連携により実施しています。
乾癬を対象とする抗体誘導ペプチドの研究については、国立研究開発法人新エネルギー・産業技術総合開発機構(NEDO)「研究開発型ベンチャー支援事業/橋渡し研究開発促進による事業化支援」の支援を受けて、橋渡し研究機関大阪大学との共同研究により実施しています(本研究は、FPP003と同じ乾癬を対象疾患としておりますが、標的タンパク質IL-23に対する探索研究であり、標的タンパク質IL-17Aに対する抗体誘導ペプチドFPP003とは別の研究開発プロジェクトであります)。
◇ 提携状況
当社は、2018年3月に、大日本住友製薬株式会社との間で、精神神経疾患を対象とする抗体誘導ペプチドの研究契約を締結しており、これに基づき、同社が探索研究を実施しております。
さらに、2019年2月に、塩野義製薬株式会社との間で、疼痛を対象とする抗体誘導ペプチドの共同研究契約を締結しております。
③ 抗ウイルス剤
◇ 提携状況
当社は、2017年5月に、富士フイルム株式会社との間でヒトパピローマウイルス(*)に対する抗ウイルス薬の共同研究契約を締結しております。
<用語解説> (50音順、アルファベット順)
|
用語 |
意味・内容 |
|
アジュバント |
主剤の免疫反応を増強する物質のことです。ワクチン製剤に含まれます。 |
|
インスリン |
膵臓から分泌されるペプチドホルモンのことです。血糖値を下げる働きをします。 |
|
液性免疫 |
「獲得免疫」の用語解説欄をご参照ください。 |
|
エピトープ |
抗体が認識して結合する抗原の特定の部位のことです。 抗原とは、一般的には、生体にとって異物である細菌、ウイルス等のタンパク質が抗原となり、生体防御として産生された抗体と抗原が結合し、生体から除去されます。一方、抗体誘導ペプチドの場合、病気に関連する自己の体内にある標的タンパク質を抗原とします。 |
|
獲得免疫 |
「獲得免疫」では、主に細菌等に対しては抗体(「液性免疫」といいます)が働き、ウイルス等に対しては細胞傷害性T細胞(「細胞性免疫」といいます)が働きます。 具体的な作用メカニズムは、病原体等の抗原を抗原提示細胞が取り込み、抗原の情報をT細胞に与え、情報を受けたヘルパーT細胞は、更にB細胞に刺激を与え、細菌等に結合する抗体をつくるように指令します。また、細胞傷害性T細胞がウイルス等に感染した細胞を攻撃します。 抗体誘導ペプチドは、病気に関連する標的タンパク質に結合してその働きを抑制する抗体(液性免疫)を産生させて効果を発揮させる一方、副作用の原因となる(標的タンパクを産生する自己細胞に対する)細胞傷害性T細胞を産生させないように設計されます。 |
|
家族性大腸腺腫症 |
大腸に多数(100個以上)の腺腫(ポリープ)が発生する遺伝性疾患です。放置すれば、40歳代で約50%、60歳頃にはほぼ100%の患者で大腸癌が発生します。 大腸癌発生予防を目的として外科的大腸切除が行われていますが、下痢や軟便、脱水、腸閉塞等の後遺症によるQOL(生活の質)低下が問題になっています。大腸切除以外の治療法として、薬物療法や内視鏡的ポリープ切除の臨床試験が行われていますが、現時点では実臨床での治療法として確立しておらず、家族性大腸腺腫症に対する新規治療法が切望されています。 |
|
キャリア |
単独では免疫を誘導できないペプチド等に結合させ、免疫反応を誘発する物質のことです。 |
|
抗体 |
外来病原菌等に結合して、その働きを抑える作用をもったタンパク質のことです。 抗体誘導ペプチドは、病気に関連する自己の体内にある標的タンパク質に結合する抗体を産生させるものです。 |
|
サイトカイン |
細胞から分泌され、細胞間相互作用に影響を与えるタンパク質のことです。 |
|
細胞傷害性T細胞 |
「獲得免疫」の用語解説欄をご参照ください。 |
|
細胞性免疫 |
「獲得免疫」の用語解説欄をご参照ください。 |
|
主要評価項目 |
臨床試験を実施するにあたり、主要な目的を評価するのに適した評価項目として設定されるものです。 |
|
尋常性疣贅(じんじょうせいゆうぜい) |
手足、膝、顔等の傷を受けやすい部位に発生する皮膚のイボで、小児期に多く発生します。 液体窒素による凍結療法やレーザー治療が行われています。 |
|
親水性 |
水に溶けやすいことです。 |
|
尖圭(せんけい)コンジローマ |
外陰部や肛門周辺等の皮膚や粘膜に発生する、先の尖った硬いイボです。性感染症として主に成人にみられます。液体窒素による凍結療法やレーザー治療に加え、イミキモド(自然免疫賦活剤)による薬物療法が行われています。 |
|
疎水性 |
水に溶けにくいことです。 |
|
肉芽 |
皮膚潰瘍が治癒する過程で形成される、赤く柔らかい粒状の結合組織のことです。 |
|
ヒトパピローマウイルス |
Human papillomavirus(HPV)。ヒトパピローマウイルスは皮膚や粘膜の傷口から接触感染するウイルス。代表的な疾患としては、尋常性疣贅(じんじょうせいゆうぜい)(*)や尖圭(せんけい)コンジローマ(*)などがあります。 |
|
プラセボ対照二重盲検ランダム化比較試験 |
「プラセボ」とは、偽薬のことです。臨床試験では、患者様が薬を使っていると思うことで症状が改善する「プラセボ効果」が生じることが指摘されています。この影響をコントロールし、開発化合物の薬理効果のみを評価するため、臨床試験では、「プラセボ」を投与した被験者群(プラセボ群)と、開発化合物を投与した被験者群(実薬群)の有効性等を比較する「プラセボ対照二重盲検」試験が行われています。 また、薬の効果は、投薬開始前の患者様の状態(病気の重症度等)により影響を受ける可能性があります。したがって、臨床試験では、プラセボ群と実薬群の間で、被験者をランダムに登録し、群間において患者様の状態のバラツキを少なくする「ランダム化(無作為化)」試験が行われています。 |
|
用語 |
意味・内容 |
|
免疫システム |
外来病原体や異物を非自己と認識し、排除しようとする生体防御システムのことです。 免疫システムには、「自然免疫」と「獲得免疫」が備わっています。通常は「自然免疫」が働いていますが、防ぎきれない場合は「獲得免疫」が働きます。 抗体誘導ペプチドは、長い期間、免疫が記憶される「獲得免疫」のメカニズムを利用しています。 |
|
用量相関 |
一般的に、薬の用量が増加すると、有効性も高くなり、一定の用量に達した段階で有効性は横ばい(プラトー)なると考えられます。この薬の用量と有効性の関係を用量相関性といいます。用量相関性は、偶然には起こりにくいことから、薬の薬理効果を推定する根拠の一つとなります。 |
|
「DESIGN-R®」合計スコア |
「DESIGN-R®」は、2008年に日本褥瘡学会が公表した褥瘡状態評価スケールであり、[深さ(Depth)]、[滲出液(Exudate)]、[大きさ(Size)]、[炎症/感染(Inflammation/Infection)]、[肉芽組織(Granulation)]、[壊死組織(Necrotic tissue)]、[ポケット(Pocket)]の7項目で評価されます。 DESIGN-R®合計スコアよる重症度判定は、重みづけした6項目(深さ(Depth)を除く)の合計スコアによって行われ、スコアが高いほど重症と判断します。
・DESIGN-R®合計スコア評価表(褥瘡経過評価用) http://www.jspu.org/jpn/info/pdf/design-r.pdf
DESIGN-R®スコア合計スコアの改善は、「1週間で1ポイント改善することにより、30日以内の褥瘡治癒確率は、浅い褥瘡で21%、深い潰瘍で23%上昇する」(Iizaka et al.(2012)(*))と考えられ、臨床的意義が高いと考えられます。 |
<参考文献> (50音順、アルファベット順)
平成22年度厚生労働科学研究補助金 免疫アレルギー疾患予防・治療研究事業 公益財団法人日本アレルギー協会事業より「的確な花粉症の治療のために」
Bachmann MF, Whitehead P. Active immunotherapy for chronic diseases. Vaccine. 2013;31:1777-84.
Bowman PH, Hogan DJ. Leg ulcers: a common problem with sometimes uncommon etiologies. Geriatrics. 1999;54:43,47-8.50 passim.
Iizaka S, Sanada H et al. Predictive validity of weekly monitoring of wound status using DESIGN-R score change for pressure ulcer healing: a multicenter prospective cohort study. Wound Repair Regen. 2012 Jul-Aug;20(4):473-81.
Jackevicius CA, Mamdani M, Tu JV. Adherence with statin therapy in elderly patients with and without acute coronary syndromes. JAMA 2002;288:462–7.
Kubota K, Kamijima Y, Sato T, et al. Epidemiology of psoriasis and palmoplantar pustulosis: a nationwide study using the Japanese national claims database. BMJ Open 2015;5: e006450. doi:10.1136/bmjopen-2014-006450
Russo A, Steiner C, Spector W. Hospitalizations Related to Pressure Ulcers among Adults 18 years and older, 2006. Healthcare Cost and Utilization Project (HCUP) Statistical Briefs [Internet]. Rockville (MD): Agency for Healthcare Research and Quality (US); 2006-.2008 Dec.
The American Academy of Dermatology website.
“Psoriasis.” https://www.aad.org/media/stats/conditions/psoriasis (Accessed August 2017)
UMIN臨床試験登録システム
https://upload.umin.ac.jp/cgi-open-bin/ctr/ctr_view.cgi?recptno=R000022106 (Accessed August 2019)
4【関係会社の状況】
該当事項はありません。
5【従業員の状況】
(1)提出会社の状況
|
2019年10月31日現在 |
|
従業員数(人) |
平均年齢(歳) |
平均勤続年数(年) |
平均年間給与(円) |
|
11 |
46.2 |
3.6 |
8,199,801 |
(注)1.従業員数は就業人員であり、使用人兼務役員を含んでおります。臨時雇用者はおりません。
2.平均年間給与は、賞与及び基準外賃金を含んでおります。
3.当社は、医薬品等の研究開発事業の単一セグメントであるため、セグメントごとの情報は記載しておりません。
(2)労働組合の状況
当社において労働組合は結成されておりませんが、労使関係は円満に推移しております。